RSS-Feed abonnieren

DOI: 10.1055/a-0897-6457
Behandlung von Patientinnen mit frühem Mammakarzinom: Evidenz, Kontroversen, Konsens
Meinungsbild deutscher Experten zur 16. Internationalen St.-Gallen-Konsensus-Konferenz (Wien 2019) Artikel in mehreren Sprachen: English | deutschCorrespondence/Korrespondenzadresse
Publikationsverlauf
received 03. April 2019
revised 20. April 2019
accepted 21. April 2019
Publikationsdatum:
14. Juni 2019 (online)
- Zusammenfassung
- Einleitung
- Operative Fragestellungen
- Operatives Vorgehen in der Axilla bei primärer Operation
- Vorgehen in der Axilla nach primär systemischer Therapie (PST)
- Teilbrust- und hypofraktionierte Bestrahlung im Fokus
- Bestrahlung der Axilla nach BET
- Strahlentherapie nach Mastektomie
- Bestrahlung nach PST – auch bei älterer Patientin
- Pathologie: TILs und PD-L1 im Fokus
- Endokrine adjuvante Therapie
- Stellenwert von Multigenexpressions-Analysen
- Adjuvante und neoadjuvante Chemotherapie
- HER2+ Mammakarzinom im Fokus
- Adjuvante „bone modifying“-Therapie
- Fertilitätserhalt
- Genetische Testung auf Hochrisiko-Mutationen?
- Schwangerschaft nach Brustkrebs
- Ernährung und Bewegung
- Duktales Carcinoma in situ (DCIS)
- Magnitude of absolute Benefit
- Anmerkung
- References/Literatur
Zusammenfassung
Die Ergebnisse der internationalen St.-Gallen-Konsensus-Konferenz zur Behandlung des primären Mammakarzinoms wurden auch dieses Jahr von einer Arbeitsgruppe führender Brustkrebsexperten vor dem Hintergrund der Therapieempfehlungen für den Klinikalltag in Deutschland diskutiert. Drei der Brustkrebsexperten sind zugleich Mitglieder des diesjährigen St.-Gallen-Panels. Der Vergleich der St.-Gallen-Empfehlungen mit den jährlich aktualisierten Therapieempfehlungen der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO-Mamma 2019) sowie der S3-Leitlinie ist sinnvoll, da die Empfehlungen des St.-Gallen-Panels ein Meinungsbild von Experten unterschiedlicher Länder und Fachdisziplinen darstellen. Die Empfehlungen der S3-Leitlinie und AGO basieren dagegen auf einer evidenzbasierten Literaturrecherche. Die diesjährige 16. St.-Gallen-Konferenz stand unter dem Motto „Magnitude of clinical benefit“. Neben der evidenzbasierten Grundlage muss jede Therapieentscheidung auch einer Nutzen-Risiko-Abwägung für die individuelle Situation einer Patientin unterzogen und mit der Patientin besprochen werden.
Schlüsselwörter
St.-Gallen-Konsensus 2019 - frühes Mammakarzinom - lokoregionäre Therapie - Axilla - neoadjuvante Therapie - SystemtherapieEinleitung
Die diesjährige 16. St.-Gallen-Konferenz zur „Primären Behandlung des frühen Mammakarzinoms“ stand unter dem Motto „Estimating the magnitude of clinical benefit of local and systemic therapies in patients with Early Breast Cancer“. Ziel war es, nicht nur den relativen Vorteil einer diagnostischen oder therapeutischen Maßnahme auf evidenzbasierter Grundlage zu bewerten, sondern die Empfehlungen auf der Grundlage des potenziellen absoluten Nutzens einer Maßnahme (und evtl. Nebenwirkungen, inklusive Langzeitschäden) in der individuellen Krankheitssituation einer Patientin mit frühem Mammakarzinom auszusprechen.
Das diesjährige St.-Gallen-Konsensus-Panel setzte sich aus mehr als 50 Brustkrebsexperten aus 23 Ländern zusammen. Fünf Panelmitglieder kamen aus Deutschland ([Tab. 1]). Die St.-Gallen-Empfehlungen basieren auf einem Votum der Panelisten. Diese beantworten die zur Abstimmung gestellten Fragen mit „ja“ (Zustimmung), „nein“ (Ablehnung) oder „Enthaltung“ (keine Stellungnahme möglich). Bei anderen Fragen geht es darum, sich zwischen mehreren, zur Wahl gestellten Optionen zu entscheiden. Ziel ist es, ein mehrheitsfähiges und praxisnahes Meinungsbild der Panelmitglieder zu erarbeiten, um im Idealfall einen internationalen Konsens für den klinischen Alltag herzustellen.
|
Vorsitz: Giuseppe Curigliano (Italien), Eric P. Winer (USA) |
||
|
Consensus Writing Committee: Harold J Burstein (USA), Marco Colleoni (Italien), Giuseppe Curigliano (Italien), Carsten Denkert (Deutschland), Peter Dubsky (Österreich/Schweiz), Michael Gnant (Österreich), Sibylle Loibl (Deutschland), Martine Piccart-Gebhart (Belgien), Philip Poortmans (Niederlande/Frankreich), Meredith Regan (USA), Hans-Jörg Senn (Schweiz), Beat Thürlimann (Schweiz), Eric P. Winer (USA) |
||
|
|
|
Da die Panelisten unterschiedliche Fachgebiete und Länder mit verschiedenen Gesundheitssystemen und Ressourcen repräsentieren, spiegelt der erzielte Konsens im Wesentlichen ein Meinungsbild dieser Experten wider, auch wenn die Abstimmungen des Panels unter Berücksichtigung der aktuell vorhandenen Evidenz erfolgen. Für eine Übersicht der Abstimmungsergebnisse siehe Beitrag: [1]. Vor diesem Hintergrund kommentiert eine deutsche Arbeitsgruppe bereits seit einigen Jahren die Abstimmungsergebnisse der St.-Gallen-Panelisten auf Basis der Therapieempfehlungen der Organkommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) [2], die ihre Empfehlungen jedes Jahr aktualisiert.
Operative Fragestellungen
Stellenwert des Schnittrandes
Im Fokus der operativen Fragestellungen stand u. a. die Bedeutung des Schnittrandes für eine mögliche Nachresektion bzw. Mastektomie, um Tumorfreiheit zu erzielen. Vor zwei Jahren – beim St.-Gallen-Konsensus-Meeting 2017 – hatte das Panel mehrheitlich abgestimmt, dass bei einem unifokalen invasiven Tumorrest die Resektion im Gesunden („no ink on tumour“) ausreicht, um auf eine Nachresektion zu verzichten. Dieses Jahr bestätigten die Panelisten dieses Votum mehrheitlich (83,3%) auch für multifokale Läsionen – unter der Voraussetzung, dass die Patientin eine adjuvante Bestrahlung erhält. Das Ergebnis der Abstimmung entspricht den aktuellen Empfehlungen der Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO Mamma) [2].
„No ink on tumour“ gilt laut Mehrheitsvotum der St.-Gallen-Panelisten (73,3%) auch für Patientinnen mit invasivem lobulären Mammakarzinom und unabhängig davon, ob eine begleitende – auch extensive (62,5%) – duktale Komponente (EIC: extended intraductal component) vorliegt. Die deutsche Expertengruppe stimmt jeweils zu und ergänzt, dass ein begleitendes duktales Carcinoma in situ (DCIS) immer „sicher“ im Gesunden (R0: mikroskopisch tumorfreier Schnittrand) entfernt werden sollte. Ein evidenzbasierter Minimalabstand ist für das extensive DCIS derzeit nicht definiert. Die deutschen Experten betonen, dass die Prognose durch den invasiven Tumor und nicht durch das DCIS beeinflusst wird.
Bei fokalem Schnittrandbefall von < 4 mm für das DCIS bzw. < 1 mm Breite für das invasive Karzinom votierte jeweils knapp die Hälfte der Panelisten (48,9 bzw. 45,5%) für eine Nachresektion, während 38,3 bzw. 43,2% diese ablehnten. Die deutsche Expertengruppe verweist darauf, dass derzeit keine Evidenz für die Indikationsstellung zu einer Nachresektion anhand einer bestimmten Ausdehnung des Tumorbefalles am Schnittrand vorliegt. Grundsätzlich sollte eine Resektion im Gesunden durchgeführt werden. In Einzelfällen und nach Diskussion des Nutzens und der Risiken der Behandlung vor dem Hintergrund der individiuellen Patientinnencharakteristika im Tumorboard kann auf eine Nachresektion verzichtet werden.
Hautmantel erhalten ja/nein?
Keinen Konsens erreichten die Panelisten bei der Frage, ob der Hautmantel bei einer Infiltration der Haut, die in der Bildgebung, aber nicht klinisch erkennbar ist, erhalten werden kann. Des Weiteren wurde diskutiert, ob der Mamillen-Areola-Komplex (MAK) bei retromamillärer Lage des Tumors erhalten werden kann. Die Fragestellung ist aus Sicht der deutschen Expertengruppe für die klinische Realität in Deutschland nicht zielführend und betrifft nur die Situation der mamillenerhaltenden Mastektomie (NSM: nipple-sparing mastectomy). Die deutschen Experten weisen darauf hin, dass bei R0-Resektion des Primärtumors der Mamillen-Areola-Erhalt möglich ist, wenn dies kosmetisch sinnvoll erscheint. Wichtig ist, die Frage der Mamillenresektion nicht allein anhand der Bildgebung, sondern klinisch und ggfs. unterstützt durch einen retroareolären Schnellschnitt zu entscheiden.
Beim inflammatorischen Mammakarzinom stimmt die deutsche Expertengruppe dem Mehrheitsvotum (83,0%) der St.-Gallen-Panelisten zu, dass die Mastektomie mit Entfernung des betroffenen Hautmantels als operativer Standard anzusehen ist. Das gilt auch für Patientinnen mit pathologisch kompletter Remission (pCR) nach primärer Systemtherapie (PST).
Operatives Vorgehen in der Axilla bei primärer Operation
Verzicht auf eine SLNB?
Die deutschen Experten und die St.-Gallen-Panelisten stimmen überein, dass präoperativ ein Ultraschall der Axilla sinnvoll ist, um zu entscheiden, ob eine Sentinel-Lymphknoten-Biopsie (SLNB) indiziert ist oder nicht.
Bei einer über 70-jährigen Patientin würde die Mehrheit (56,5%) der St.-Gallen-Panelisten bei klinisch unauffälligem Nodalstatus (cN0) und kleinem (T1) Luminal-A-Karzinom auf die SLNB verzichten. Über 80% der Panelisten plädierten dafür, dies auch bei einer älteren Patientin nur aufgrund von Komorbiditäten mit reduzierter Lebenserwartung zu tun und nicht wegen des Alters per se. Für Patientinnen mit einem T2-Karzinom (Luminal A-like) lehnten 89,4% der St.-Gallen-Panelisten den Verzicht auf eine SLNB ab.
Die deutsche Expertengruppe weist darauf hin, dass die SLNB derzeit als Standardverfahren für alle Patientinnen mit einem klinisch nodal-negativen invasiven Mammakarzinom (cN0) anzusehen ist. Dies gilt auch für Patientinnen mit kleinem Karzinom (cT1) und einem Luminal-A-like-Subtyp und gilt grundsätzlich unabhängig vom Lebensalter der Patientin. Laut AGO-Empfehlung [2] sollten ältere Patientinnen mit einer Lebenserwartung von mindestens 5 Jahren die gleiche Therapie wie jüngere Patientinnen erhalten. Bei klinisch relevanten Komorbiditäten oder einer Lebenserwartung von unter 5 Jahren kann von diesem Standardvorgehen abgewichen und auf eine SLNB verzichtet werden. Jede Patientin sollte dies nach entsprechender Aufklärung und einer sorgfältigen Nutzen-Risiko-Abwägung selber entscheiden können. Die Daten der randomisierten Studien INSEMA [3] und SOUND [4] sollten vor einer Änderung der geltenden Therapiestandards abgewartet werden. Diese Studien vergleichen eine Sentinel-Biopsie vs. keine axilläre Operation bei Patientinnen mit klinisch unauffälliger Axilla und geplanter brusterhaltender Operation.
Vorgehen in der Axilla bei positivem Sentinel-Lymphknoten
Für Patientinnen mit einem positivem Sentinel-Lymphknoten (SN) wurde das therapeutische Vorgehen in der Axilla anhand verschiedener Szenarien diskutiert – axilläre Lymphknotendissektion (ALND) nach Mastektomie bzw. brusterhaltender Operation, wenn die ACOSOG-Kriterien (siehe [5]) nicht erfüllt sind, und Stellenwert der Bestrahlung, wenn auf eine ALND verzichtet wird.
Eine einfache Mehrheit (47,9%) der St.-Gallen-Panelisten würde bei einer Patientin mit einem T1/2-Mammakarzinom und 1 – 2 makrometastatisch befallenen SN (SN+) nach Mastektomie eine Bestrahlung der Axilla (LAG: Lymphabflussgebiete) nach AMAROS durchführen (siehe [6]) – vorausgesetzt, dass adjuvant eine systemische Standardtherapie geplant ist. Keine zusätzliche Intervention (Operation oder Bestrahlung) in der Axilla empfehlen 12,5%; 16,7% votierten dafür, die ALND zu komplettieren.
Die deutsche Expertengruppe stimmt dem Votum nicht zu. Sie verweist zunächst darauf, dass eine weitere Behandlung der Axilla in dieser Situation notwendig ist. Drei Therapieoptionen stehen zur Verfügung: Im Rahmen einer Tangentialfeld-Bestrahlung (PMRT: Post-Mastektomie-Radiotherapie) ist eine Bestrahlung der Thoraxwand mit Tangente bis 5 mm unterhalb der V. axillaris (ohne ALND) möglich. Die weiteren Optionen sind die Bestrahlung des Lymphabflussgebietes nach AMAROS [6] oder eine ALND. Das optimale Vorgehen in dieser Situation – nach Mastektomie – wird derzeit noch in den kontrollierten klinischen Studien untersucht. Ist eine Strahlentherapie der Thoraxwand geplant, kann möglicherweise auf eine ALND verzichtet werden, wenn die Strahlentherapie auf die Axilla ausgedehnt wird.
Laut Mehrheitsvotum der St.-Gallen-Panelisten kann bei Patientinnen nach Mastektomie mit makrometastatisch befallenen SN in folgenden Situationen auf eine ALND verzichtet werden:
-
Patientin mit triple-negativem Mammakarzinom (TNBC) und 1 – 2 positiven SN, wenn eine Bestrahlung des LAG geplant ist (Mehrheitsvotum: 70,8%).
-
Patientin mit 1 – 2 positiven SN, positivem Östrogenrezeptor- (ER+) und positivem HER2-Status (HER2+) sowie geplanter Bestrahlung des LAG (Mehrheitsvotum: 83,3%).
Dagegen lehnten die Panelisten den Verzicht auf eine ALND mehrheitlich ab, wenn bei Patientinnen nach Mastektomie mit 1 – 2 positiven SN eine Bestrahlung der Thoraxwand, nicht aber des LAG geplant ist (Mehrheitsvotum: 66,0%).
Die deutsche Expertengruppe weist erneut darauf hin, dass bei einer Patientin mit Mastektomie und 1 – 2 befallenen SLN grundsätzlich eine weitere Behandlung der Axilla in Form einer Bestrahlung oder operativ (ALND) erforderlich ist. Dies gilt unabhängig vom intrinsischen Subtyp. Derzeit laufende Studien, u. a. zu den Zielvolumina und der Strahlendosis, müssen abgewartet werden, um eine eindeutige und evidenzbasierte Empfehlung aussprechen zu können.
ALND nach primärer BET?
Knapp zwei Drittel (60,9%) der St.-Gallen-Panelisten lehnten den Verzicht auf eine ALND bei Patientinnen mit einem Primärtumor > 5 cm und 1 – 2 positiven SN ab, die brusterhaltend operiert wurden und eine Ganzbrustbestrahlung (WBRT) erhalten. Die deutsche Expertengruppe stimmt zu, da die ACOSOG-Kriterien in dieser Situation nicht erfüllt sind [5].
Erhalten die gleichen Patientinnen (T > 5 cm, 1 – 2 SN+, BET, WBRT) zusätzlich eine Bestrahlung der regionären Lymphknoten, ist laut Mehrheitsvotum der Panelisten (73,9%) ein Verzicht auf die ALND möglich. Die deutsche Expertengruppe verweist auf die unzureichende Datenlage. Sie stimmt dem Votum der Panelisten im Analogieschluss zu den AMAROS-Daten [6] im Sinne einer Zustimmung auf „Expertenlevel“ zu.
Strahlentherapie bei Verzicht auf die ALND
Eine einfache Mehrheit (41,7%) der St.-Gallen-Panelisten votierte dafür, dass eine Patientin mit primärem Mammakarzinom (T < 5 cm) und 1 – 2 (makrometastatisch) befallenen Sentinel-Lymphknoten (SN), die brusterhaltend operiert wurde, aber keine ALND erhalten hat, eine Ganzbrustbestrahlung ohne zusätzliche Bestrahlung der Axilla (keine hohe Tangente) erhalten sollte – die deutsche Expertengruppe stimmt mit Verweis auf die AGO-Empfehlung [2] nicht zu. Danach wird in diesem Fall eine Tangential-Feldbestrahlung der Brust bis 5 mm unterhalb der V. axillaris empfohlen, welche die Level 1 und 2 weitgehend einschließt ([Abb. 1]).


Vorgehen in der Axilla nach primär systemischer Therapie (PST)
cN1-Situation nach PST
Das Votum zur Frage, wann bei einer Patientin mit klinisch positivem Nodalstatus (cN1), die nach PST unauffällige Lymphknoten (ycN0) aufweist, die alleinige SLNB für die Festlegung des ypN-Stadiums ausreicht, wird aus deutscher Sicht nicht unterstützt: Gut die Hälfte der St.-Gallen-Panelisten (54,2%) votiert dafür, dass ein Verzicht auf die ALND bei Nachweis von 1 – 2 negativen SN möglich ist (43,8% stimmten nicht zu), während fast alle Panelisten (91,7%) bei 3 und mehr negativen SN die alleinige SLNB für ausreichend ansahen.
Die deutsche Expertengruppe stimmt nicht zu, da bei 1 – 2 negativen SNs die falsch negative Rate (FNR) zu hoch ist. Die deutschen Experten empfehlen mit Verweis auf die Empfehlungen der AGO Mamma [2], dass bei der Planung einer neoadjuvanten Therapie bei initial positiven Lymphknoten eine TAD („targeted“ Axilladissektion) mit vorheriger Clip-Markierung des stanzbioptisch gesicherten Lymphknotens angestrebt werden sollte. Bei 3 und mehr im Schnellschnitt negativen SNs kann dagegen auf eine ALND verzichtet werden. Die deutschen Experten verweisen darauf, dass die FNR bei 1 – 2 entfernten SN > 10% und bei 3 entfernten SN < 10% liegt und dass zur Erhöhung der Anzahl resezierter Lymphknoten (mit dem Ziel der Erreichung einer FNR < 10%) keine Nicht-SNs entfernt werden sollten.
Wurde im genannten Kollektiv der Lymphknoten prätherapeutisch markiert und ist dieser Target-Lymphknoten (TLN) nach PST tumorfrei, votierten die St.-Gallen-Panelisten nur dann mehrheitlich (92,1%) für den Verzicht auf eine ALND, wenn zusätzliche SNs entfernt wurden und auch diese negativ waren. Die AGO Mamma empfiehlt in dieser Situation, den (die) SLNs sowie den TLN (i. S. einer TAD) zu entnehmen. Sind diese Lymphknoten tumorfrei, kann auf eine ALND verzichtet werden. Derzeit werden verschiedene Validierungsstudien durchgeführt, um die Reproduzierbarkeit des Verfahrens zu zeigen.
Die St.-Gallen-Panelisten (Mehrheitsvotum 63,8%) und die deutschen Experten sind sich einig, dass bei einer Patientin, die bei Erstdiagnose einen histologischen Nodalbefall aufweist, auch dann eine ALND erforderlich ist, wenn die Patientin gut auf die PST angesprochen hat, aber bei der SLNB mindestens 1 von 3 detektierten SNs Mikrometastasen aufweist und bei der Patientin keine Bestrahlung geplant ist. In dieser Situation besteht ein hohes Risiko, dass über den SN hinaus weitere Lymphknoten metastatisch befallen sind.
Bestrahlung der Lymphabflussgebiete nach PST
Mehrheitlich (43,8%) votierten die St.-Gallen-Panelisten dafür, dass die klinisch nodal-positive Patientin (cN+) mit negativem SN nach PST standardmäßig eine Bestrahlung der LAG erhalten sollte. Knapp 17% sehen in der Bestrahlung der LAG keinen Standard und 22,9% votierten nur dann für eine LAG-Bestrahlung, wenn Risikofaktoren, wie beispielsweise ein großer Primärtumor, eine vaskuläre Infiltration, eine hohe Anzahl verdächtiger LK bei Erstdiagnose u. a. vorliegen. Die deutsche Expertengruppe stimmt dem letzten Votum der St.-Gallen-Panelisten grundsätzlich zu. Ein Verzicht auf die LAG-Bestrahlung ist in dem genannten Kollektiv (CR: ypT0/is ypN0) nach PST nur bei Patientinnen mit kompletter Remission (pCR) (ypT0/is ypN0) möglich. Die deutschen Experten verweisen auf die Empfehlungen der AGO Mamma ([Abb. 2]) [2].


Teilbrust- und hypofraktionierte Bestrahlung im Fokus
Die deutsche Expertengruppe stimmt dem einfachen Mehrheitsvotum (43,8%) der St.-Gallen-Panelisten zu, dass die (akzelerierte) Teilbrustbestrahlung (PBI: partial breast irradiation) eine Option für Patientinnen ist, die gemäß der Definition der ASTRO (American Society of Radiation-Oncology) und GEC-ESTRO (Groupe Européen de Curiethérapie-European Society for Radiotherapy & Oncology) als geeignet („suitable“) eingestuft werden und ein niedriges Rückfallrisiko haben [7], [8], [9], [10].
Die St.-Gallen-Panelisten sehen mehrheitlich (52,1%) in der hypofraktionierten Bestrahlung der Brust und der Thoraxwand ein Standardvorgehen für grundsätzlich alle Patientinnen, bei denen eine adjuvante Nachbestrahlung indiziert ist. Ausgenommen werden seltene Situationen wie eine Zweitbestrahlung. Die deutsche Expertengruppe stimmt diesem Votum explizit für die brusterhaltende Operation zu und verweist auf die unzureichende Datenlage hinsichtlich der Thoraxwandbestrahlung. Die deutschen Experten verweisen auf die Empfehlungen der AGO Mamma [2].
Wenig eindeutig ist das Votum der St.-Gallen-Panelisten, ob die hypofraktionierte Bestrahlung auch für die Bestrahlung der LAG gelten sollte. Nur 36,2% sehen hierin ein Standardvorgehen. Knapp 30% (29,8%) sprachen sich explizit dagegen aus und genauso viele Panelisten enthielten sich der Stimme. Auch aus deutscher Sicht ist die hypofraktionierte Bestrahlung der regionalen Lymphknoten kein Standardvorgehen.
Bestrahlung der Axilla nach BET
Nach BET sollte die Bestrahlung der Lymphabflussgebiete immer dann die nicht axillären Lymphknoten (supraklavikulär ± Mammaria-interna-Region) erfassen, wenn mindestens 4 axilläre Lymphknoten befallen sind, so das Votum (93,8%) der St.-Gallen-Panelisten. Sind „nur“ 1 – 3 axilläre Lymphknoten befallen, sollten nur dann alle regionalen Lymphabflussgebiete von der Bestrahlung erfasst werden, wenn zusätzlich prognostisch ungünstige Eigenschaften vorliegen wie z. B. ein triple-negatives Mammakarzinom (TNBC) oder ein Tumorrest nach PST, so das Mehrheitsvotum (56,2%) der Panelisten. Die deutsche Expertengruppe stimmt jeweils zu.
Strahlentherapie nach Mastektomie
Die adjuvante Bestrahlung nach Mastektomie umfasst die Bestrahlung der Thoraxwand und der LAG. Der Stellenwert der PMRT wurde anhand verschiedener Szenarien abgestimmt. Die Frage, ob eine PMRT bei Patientinnen mit einem pT3 pN0-Karzinom als Standard anzusehen ist, bejahten die St.-Gallen-Panelisten mit knapper Mehrheit (56,2 vs. 43,8%). In einer zusätzlichen (spontanen) Abstimmung vor Ort votierten 54,3% der Panelisten für eine „case-by-case“-Entscheidung. Die deutsche Expertengruppe schränkt mit Verweis auf die Empfehlungen der AGO Mamma [2] ([Abb. 3]) ein, dass dies nur für pT3pN0-Patientinnen mit zusätzlichen Risikofaktoren gilt und plädierte ebenfalls für eine individuelle Entscheidung im Tumorboard.


Die Frage, ob eine PMRT nur bei pT2 pN0-Karzinomen mit ungünstigen Faktoren ein Standardvorgehen ist, verneinten die St.-Gallen-Panelisten mehrheitlich (63,8%), ebenso wie die deutschen Experten.
Kein Mehrheitsvotum erreichten die St.-Gallen-Panelisten für die PMRT bei Patientinnen mit 1 – 3 befallenen Lymphknoten (N+ 1 – 3) und positivem ER- und/oder HER2-Status (ER+ und/oder HER2+). Über 85% der St.-Gallen-Panelisten sehen jedoch in der PMRT ein Standardvorgehen bei Patientinnen mit N+ 1 – 3 und ungünstigen Eigenschaften (z. B. bei einem TNBC). Die deutsche Expertengruppe stimmt diesem letzten Votum zu und verweist darüber hinaus auf die AGO-Empfehlungen der Kommission Mamma ([Abb. 4]) [2].


Eine Mehrheit (66,0%) der St.-Gallen-Panelisten sieht auch bei 1 – 2 positiven SN eine standardmäßige Indikation für eine PMRT, wenn die Patientin keine PST und keine ALND erhalten hat. Die deutsche Expertengruppe verweist darauf, dass eine PMRT bei diesen Patientinnen grundsätzlich indiziert ist, wenn keine ALND erfolgte.
Eine deutliche Mehrheit der St.-Gallen-Panelisten (75%) und die deutsche Expertengruppe stimmen auch darin überein, dass die Indikation für eine PMRT unabhängig davon besteht, ob eine primäre Brustrekonstruktion vorgenommen wird oder nicht.
Bestrahlung nach PST – auch bei älterer Patientin
Gemäß der aktuellen Datenlage – u. a. retrospektiv – sollte eine „gesunde“ Patientin mit TNBC im Stadium T3N0, die auf die PST gut angesprochen hat (z. B. pCR bei Mastektomie mit einem 6 cm großen tumorfreien Tumorbett ohne befallenen SN) eine PMRT erhalten, da sich die Therapieentscheidung am Ausgangsrisiko orientiert.
Fast 55% (54,2%) der St.-Gallen-Panelisten votierten dafür, dass eine „gesunde“ 70-jährige Patientin, deren Mammakarzinom (Stadium I, ER+) im Rahmen der Früherkennung entdeckt und die brusterhaltend operiert wurde, eine postoperative Bestrahlung und eine adjuvante endokrine Therapie erhalten sollte. 35,4% der Panelisten würden nur endokrin weiter behandeln. Ist die gleiche Patientin bereits über 80 Jahre alt, wären 62,2% der St.-Gallen-Panelisten mit der adjuvanten Weiterbehandlung zurückhaltender.
Die deutsche Expertengruppe stimmt diesem Trend zu, dass bei höherem Lebensalter und potenziell geringer Lebenserwartung eine reduzierte Behandlung sinnvoll sein kann. Grundsätzlich weisen die deutschen Experten aber darauf hin, dass das Lebensalter per se kein Kriterium für die Therapieentscheidung ist. Entscheidend sind Komorbiditäten und die verbleibende Lebenserwartung, wenn über eine reduzierte Therapie nachgedacht wird. Eine Beratung durch einen Strahlentherapeuten ist hier dennoch zu empfehlen.
Pathologie: TILs und PD-L1 im Fokus
Der Stellenwert der tumorinfiltrierenden Lymphozyten (TILs) für die Therapieentscheidung wird seit Jahren diskutiert. Die deutsche Expertengruppe stimmt dem Votum der St.-Gallen-Panelisten, die TILs bei Patientinnen mit TNBC routinemäßig zu bestimmen, nicht zu. Ein hoher TIL-Prozentsatz impliziert nicht, dass auf eine Chemotherapie verzichtet werden kann. Die deutschen Experten betonen, dass sich aus der TIL-Bestimmung derzeit keine therapeutischen Konsequenzen ergeben.
Vor dem Hintergrund der IMpassion 130-Studie [11], [12] und der US-amerikanischen Zulassung des ersten PD-L1-(programmed-cell-death-ligand1-)Checkpoint-Inhibitors beim metastasierten PD-L1-positiven TNBC (in Kombination mit nab-Paclitaxel) wird diskutiert, die PD-L1-Expression zu bestimmen. Die routinemäßige Bestimmung der PD-L1-Expression beim frühen TNBC lehnten die St.-Gallen-Panelisten mehrheitlich (79,2%) ab. Das gilt auch für die Bestimmung auf den Immunzellen (Mehrheitsvotum 91,5%), die in der metastasierten Situation die Therapieindikation unterstützt. Die deutsche Expertengruppe stimmt beiden Voten zu.
Stellenwert der Multigenexpressions-Analysen
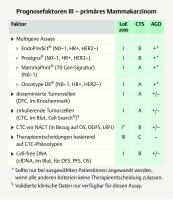
Multigenexpressions-Analysen können bei Patientinnen mit ER+/HER2− frühem Mammakarzinom die Therapieentscheidung für bzw. gegen eine Chemotherapie-Indikation unterstützen. Die St.-Gallen-Panelisten empfehlen den Einsatz von Multigenexpressions-Analysen zu über 90% für Patientinnen mit einem T1/2-Karzinom ohne Lymphknotenbefall (93,6%), aber mehrheitlich auch für jene mit T3N0-Karzinom (74,5%) sowie unabhängig vom T-Stadium für Patientinnen mit 1 – 3 befallenen Lymphknoten (78,7%). Die deutsche Expertengruppe schränkt ein, dass Multigenexpressions-Analysen nur dann zum Einsatz kommen sollten, wenn die klassischen klinischen Parameter keine ausreichende Basis einer Therapieentscheidung für bzw. gegen eine Chemotherapie bieten ([Abb. 5]) [2]. Bei Patientinnen mit Lymphknotenbefall ist der klinische Wert der Multigenexpressions-Analysen bisher nicht im Rahmen von prospektiven Studien nachgewiesen, sodass hier kein Stellenwert von Multigenexpressions-Analysen gesehen wird.

Endokrine adjuvante Therapie
Die endokrine adjuvante Behandlung ist Therapie der Wahl für Patientinnen mit ER+ (hormonsensiblem) Mammakarzinom [2]. Der ideale „Cut-off“-Wert für eine Indikation zu einer endokrinen Therapie liegt laut einfachem Mehrheitsvotum (38,8%) der Panelisten bei ER > 10%. Knapp 25% der Panelisten gaben an, dass der Cut-off nicht klar definiert ist, und 30,1% sahen den Cut-off bei ER > 1%.
Das Votum verdeutlicht, dass es keinen idealen „Cut-off“-Wert gibt. Aus deutscher Sicht besteht ab einem ER-Wert ≥ 1% formal eine Indikation für eine endokrine Therapie, weshalb diese bei ER ≥ 1% im Tumorboard diskutiert und mit der Patientin besprochen werden sollte – u. a. in Abhängigkeit vom Alter der Patientin und zusätzlichen Prognosefaktoren.
Selektionsfaktoren in der Prämenopause
Für prämenopausale Patientinnen mit einem frühen ER+ Mammakarzinom ist die ovarielle Suppression (OFS [ovarian function suppression]: GnRH-Analoga oder durch bilaterale Ovarektomie) zusätzlich zu Tamoxifen oder einem Aromatasehemmer (AI) eine Option. Eine Indikation für eine zusätzliche OFS sehen zwei Drittel (68,1%) der St.-Gallen-Panelisten immer dann, wenn bei hohem Rückfallrisiko auch eine Chemotherapie-Indikation besteht. Die deutsche Expertengruppe stimmt zu.
Weitere klinisch-pathologische Faktoren, die eine OFS-Indikation „by itself“ begründen, also ohne dass weitere Faktoren vorliegen müssen, sehen die Panelisten mehrheitlich bei jungen Patientinnen ≤ 35 Jahre (84,8%) sowie zu fast 60% (59,6%) auch bei einem abweichenden Ergebnis einer Multigenexpressions-Analyse. Die deutsche Expertengruppe stimmt beiden Voten nicht zu: Das junge Lebensalter per se ist wahrscheinlich keine zwingende Indikation für eine OFS. Zu Multigenexpressions-Analysen und deren Aussage bezüglich einer Eskalation der endokrinen Therapie gibt es bisher keine Daten.
Einigkeit besteht, dass weder ein moderates Risiko ohne Chemotherapie-Indikation noch ein positiver HER2-Status eine OFS-Indikation begründen. Das gilt aus deutscher Sicht auch für den Lymphknotenbefall. Die entscheidende Voraussetzung für die Indikation zu einer OFS ist die persistierende Ovarialfunktion nach (neo)adjuvanter Chemotherapie sowie das Rückfallrisiko. Dies ist ab 4 befallenen Lymphknoten immer der Fall und hängt bei 1 – 3 befallenen Lymphknoten von den weiteren Risikofaktoren ab. Insofern stimmen die deutschen Experten der einfachen Mehrheit (37,8%) der St.-Gallen-Panelisten nicht zu, dass bereits ein befallener Lymphknoten (per se) eine OFS-Indikation rechtfertigt.
Die St.-Gallen-Panelisten (55,1%) und die deutsche Expertengruppe stimmen überein, dass eine OFS bei bestehender Indikation idealerweise über 5 Jahre erfolgen sollte [13]. Bei AI-Gabe ist die zusätzliche OFS bei der prämenopausalen Patientin obligat. Unter Tamoxifen kann die OFS vorzeitig beendet werden, falls dies z. B. wegen Nebenwirkungen notwendig ist.
Endokrine Therapie in der Postmenopause
Postmenopausale Patientinnen mit ER+ frühem Mammakarzinom sollten irgendwann im Therapieverlauf einen AI erhalten. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum (95,7%) der Panelisten zu. Ein G3-Karzinom, ein hoher Ki-67-Wert oder ein positiver HER2-Status sind Indikationen für einen AI. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum der Panelisten zu, verweist aber darauf, dass die genannten Faktoren keine prädiktiven Faktoren für den Nutzen einer AI-Gabe sind, sondern lediglich ein erhöhtes Rückfallrisiko implizieren. Einigkeit besteht, dass der AI nicht notwendigerweise von Anfang an („upfront“) eingesetzt werden muss. Eine „Upfront“-Gabe des AI wird jedoch bei erhöhtem Risiko aufgrund eines fortgeschrittenen Tumorstadiums empfohlen.
Therapie der prämenopausalen Patientin nach 5 Jahren Tamoxifen
Bei Brustkrebspatientinnen im Stadium I, die nach erfolgreicher 5-jähriger Tamoxifen-Therapie nach wie vor prämenopausal sind, sollte die Behandlung laut Mehrheitsvotum der Panelisten (54,3%) beendet werden. Für eine Weiterbehandlung mit Tamoxifen über weitere 5 Jahre votierten 37,0% der Panelisten. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum (Therapie-Stopp) zu, weist aber darauf hin, dass in dieser Situation Einzelfallentscheidungen u. a. in Abhängigkeit vom Sicherheitsbedürfnis der Patientin möglich sind.
Prämenopausale Patientinnen, die sich bei Erstdiagnose im Stadium II befinden und befallene Lymphknoten aufweisen, sollten dagegen über weitere 5 Jahre – also insgesamt 10 Jahre – Tamoxifen erhalten (79,6%). Keiner der Panelisten votierte in dieser Situation mit erhöhtem Ausgangsrisiko für eine Beendigung der Therapie. Die deutsche Expertengruppe stimmt zu.
Erweiterte endokrine Therapie in der Postmenopause
Eine über 5 Jahre hinausgehende endokrine Therapie setzt voraus, dass die Behandlung in den ersten 5 Jahren ausreichend gut vertragen wurde. Unter dieser Prämisse kann die sog. erweiterte endokrine Therapie für Patientinnen mit ER+ Mammakarzinom im Stadium II eine Option sein. Mehrheitlich empfahlen die Panelisten die erweiterte endokrine Therapie für folgende Situationen:
-
Patientinnen im Stadium II, die in den ersten 5 Jahren mit Tamoxifen behandelt wurden – unabhängig vom Lymphknotenbefall bei Erstdiagnose (N0: 68,1%, N+: 97,9%).
-
Patientinnen im Stadium II mit Lymphknotenbefall bei Erstdiagnose, die über 5 Jahre mit einem AI behandelt wurden (81,2%).
Keine Indikation für eine erweiterte endokrine Therapie sieht die Mehrheit der Panelisten für diese Patientinnen:
-
Patientinnen im Stadium I – unabhängig davon, welche endokrine Vortherapie (Tamoxifen oder AI) eingesetzt wurde.
-
Patientinnen im Stadium II, wenn bei Erstdiagnose kein Lymphknotenbefall vorlag und die Patientinnen 5 Jahre einen AI hatten.
Die deutsche Expertengruppe stimmt den Abstimmungsergebnissen jeweils zu, verweist aber darauf, dass die erweiterte endokrine Therapie auch bei Patientinnen mit vermeintlich niedrigem Risiko (Stadium I bzw. Stadium II [N0, AI-Upfront-Therapie über 5 Jahre]) im Einzelfall – abhängig von der Risiko-Nutzen-Abwägung und dem Patientenwunsch – nach sorgfältiger Aufklärung eine Option sein kann.
Knapp 60% der Panelisten votierten dafür, die erweiterte endokrine Therapie über 5 Jahre zu empfehlen, entsprechend einer Gesamt-Therapiedauer von 10 Jahren; knapp ein Drittel (31,7%) votierte für eine Gesamt-Therapiedauer von 7 – 8 Jahren. Aus deutscher Sicht hängt die Therapiedauer von der endokrinen Vortherapie ab und sollte entsprechend differenziert werden: Eine Gesamt-Therapiedauer über 10 Jahre ist aus deutscher Sicht eine Option für Patientinnen mit 5-jähriger Tamoxifen-Vorbehandlung. Hatten Patientinnen in den ersten 5 Jahren bereits einen AI, wird die erweiterte endokrine Behandlung vorzugsweise über 2 – 3 Jahre fortgeführt, entsprechend einer Gesamt-Therapiedauer von 7 – 8 Jahren. Für Patientinnen mit einem besonders hohen Rückfallrisiko (z. B. ≥ 10 befallene Lymphknoten, G3 etc.) ist allerdings eine erweiterte endokrine Therapie über mehr als 10 Jahre eine Option.
Chemotherapie-Indikation beim Niedrigrisiko-Karzinom?
Eine Indikation für eine adjuvante Chemotherapie besteht laut Mehrheit der St.-Gallen-Panelisten (64,6%), wenn bei Erstdiagnose 4 – 9 Lymphknoten befallen sind. Das gilt auch beim Luminal-A-Mammakarzinom (ER+/HER2−, G1) sowie beim „klassischen“ lobulären Mammakarzinom. Die deutsche Expertengruppe stimmt zu.
Stellenwert von Multigenexpressions-Analysen
Die St.-Gallen-Panelisten stimmten in diesem Jahr nicht mehr über einzelne Multigenexpressions-Signaturen ab. Ein Teil der Abstimmungen bezog sich auf die prospektiven Studien, wie z. B. die TAILORx- [14] oder die MINDACT-Studie [15]. Die deutsche Expertengruppe weist darauf hin, dass laut Empfehlung der AGO Mamma bei entsprechender Indikation jede der 4 verfügbaren Multigenexpressions-Signaturen – OncotypeDX® Recurrence Score (RS), MammaPrint 70® (MP), Prosigna® PAM 50 Risk of Recurrence Score (ROR), EndoPredict® (EP) – eingesetzt werden kann ([Abb. 5]) [2].
Patientinnen ohne Lymphknotenbefall
Laut TAILORx-Studie [14] benötigen Patientinnen ohne Lymphknotenbefall und einem Recurrence Score (RS) ≤ 25 keine Chemotherapie. Bei prämenopausalen Patientinnen (< 50 Jahre) mit einem RS 21 – 25 sieht eine knappe Mehrheit (52,1%) der Panelisten eine Chemotherapie-Indikation zusätzlich zur endokrinen Therapie ± OFS. Für die zusätzliche OFS votierten 10,4% der Panelisten. Ein Viertel der Panelisten sieht eine zusätzliche OFS-, aber keine Chemotherapie-Indikation.
Die deutsche Expertengruppe bestätigt die Chemotherapie-Indikation bei diesen Patientinnen. Ist die Patientin nach Chemotherapie prämenopausal, sollte aus deutscher Sicht zusätzlich zur endokrinen Therapie eine OFS erfolgen. Besteht eine eindeutig postmenopausale Situation, sollte im Anschluss an die Chemotherapie eine endokrine Therapie ohne OFS eingesetzt werden.
Ob eine postmenopausale Patientin ohne Lymphknotenbefall und einem RS ≥ 26 eine Chemotherapie erhalten sollte, machten 57,1% der Panelisten von weiteren histopathologischen Kriterien sowie dem Wunsch der Patientin abhängig. Für einen routinemäßigen Einsatz der Chemotherapie stimmten in dieser Situation 38,8% der Panelisten. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum zu, dass weitere histopathologische Kriterien bei der Therapieentscheidung zu berücksichtigen sind.
Patientinnen mit Lymphknotenbefall
In der Plan B- [16] und der MINDACT-Studie [15] wurden der RS bzw. MP (MammaPrint) auch bei Patientinnen mit Lymphknotenbefall validiert. Vor dem Hintergrund der Plan-B-Studie verneint eine Mehrheit (78,7%) der Panelisten eine adjuvante Chemotherapie-Indikation bei Patientinnen mit einem RS < 11 bzw. bei Patientinnen > 50 Jahre und 1 – 2 befallenen Lymphknoten. Die deutsche Expertengruppe merkt an: Da in die Plan-B-Studie prä- und postmenopausale Patientinnen randomisiert wurden, ist eine altersabhängige Unterteilung schwierig. Ob bei jüngeren Patientinnen (< 50 Jahre) mit 1 – 2 befallenen Lymphknoten und niedrigem RS (RS < 11) auf eine adjuvante Chemotherapie verzichtet werden kann, wurde im deutschen Expertengremium kontrovers diskutiert. Die Hälfte spricht sich dafür und die andere Hälfte dagegen aus.
Keine Indikation für eine adjuvante Chemotherapie besteht vor dem Hintergrund der MINDACT-Studie [15] bei Patientinnen mit niedrigem Risiko (MP-Score) und 1 – 2 befallenen Lymphknoten. Hier waren sich die Panelisten und die deutsche Expertengruppe einig, dass dies altersunabhängig sowohl für Patientinnen < 50 Jahre (Mehrheitsvotum: 78,7%) als auch jene > 50 Jahre (Mehrheitsvotum: 80,9%) gilt. Die deutsche Expertengruppe verweist auch auf die Empfehlung der AGO Mamma [2], wonach in Deutschland nicht zwischen den verfügbaren, klinisch validierten, kommerziellen Testsystemen unterschieden wird ([Abb. 5]).
Neoadjuvante endokrine Therapie?
Für postmenopausale Patientinnen ist die neoadjuvante endokrine Therapie gegenüber einer neoadjuvanten Chemotherapie zu bevorzugen, wenn ein Luminal A-ähnlicher Subtyp vorliegt, der immunhistochemisch oder mittels Multigenexpressions-Analyse bestätigt wurde und eine endokrine Therapie nahelegt, so das Mehrheitsvotum der Panelisten (81,2%), dem die deutsche Expertengruppe zustimmt. Einigkeit besteht auch, dass die neoadjuvante endokrine Therapie so lange durchgeführt werden sollte, bis eine optimale Reduktion der Tumorlast erreicht ist, das heißt in der Regel mindestens über 6 Monate.
Adjuvante und neoadjuvante Chemotherapie
Chemotherapie bei ER+/N0-Patientinnen
Patientinnen mit einem ER+ Mammakarzinom ohne Lymphknotenbefall (N0) sollten bei Chemotherapie-Indikation laut Mehrheitsvotum der Panelisten (54,2%) vorzugsweise eine Chemotherapie mit einem Taxan plus einem Alkylans erhalten. Dies entspricht nicht der AGO-Empfehlung [2]. In Deutschland werden Anthrazyklin-/Taxan-basierte Regime plus ein Alkylans bevorzugt. Im Einzelfall – z. B., um Nebenwirkungen der Anthrazykline zu umgehen – kann ein Anthrazyklin-freies Regime eingesetzt werden, wie die Kombination Docetaxel/Cyclophosphamid (TC).
Chemotherapie beim TNBC
Beim TNBC bevorzugt die Mehrheit der St.-Gallen-Panelisten in Übereinstimmung mit der AGO Mamma [2] ab Stadium I (Stadium I: 77,6%: Stadium II oder III: 93,3%) ein Anthrazyklin-/Taxan-basiertes Regime plus ein Alkylans. Bei einem pT1a/b-TNBC würden die Panelisten allerdings mehrheitlich (52,2%) auf das Anthrazyklin verzichten. Laut Empfehlung der AGO Mamma ist ein Alkylans-/Taxan-basiertes Regime ± Anthrazyklin eine evidenzbasierte Option [2]. Die deutschen Experten ergänzen, dass beim TNBC der neoadjuvante Einsatz der Chemotherapie aufgrund der prognostisch wichtigen Überprüfung des Ansprechens zu bevorzugen ist. Anthrazyklin-/Taxan-basierte Regime sollten im (neo)adjuvanten Setting vorzugsweise dosisdicht eingesetzt werden, so das Mehrheitsvotum der Panelisten (61,0%), dem die deutsche Expertengruppe zustimmt ([Abb. 6]) [2].


Neoadjuvanter Einsatz von Platin?
Der neoadjuvante Einsatz von Platin wird beim TNBC immer wieder diskutiert. Unter platinhaltiger neoadjuvanter Chemotherapie wird eine höhere pCR-Rate erreicht [17], [18], [19], [20]. In der GeparSixto-Studie hat sich die höhere pCR-Rate für die Gesamtheit der TNBC-Patientinnen – unabhängig vom BRCA1/2-Status – in ein längeres DFS übertragen (p < 0,001) [19]. Die AGO Mamma empfiehlt den neoadjuvanten Einsatz von Platin bei erhöhtem Risiko (hohe Tumorlast, schlechtes Ansprechen) ([Abb. 6]). Die deutsche Expertengruppe stimmt daher den St.-Gallen-Panelisten nicht zu, die mehrheitlich (56,5%) den neoadjuvanten Einsatz von Platin zusätzlich zu einem Anthrazyklin-/Alkylans-/Taxan-basierten Regime ablehnen.
Ebenfalls keine Zustimmung der deutschen Expertengruppe gibt es zum Mehrheitsvotum der Panelisten (67,3%), den neoadjuvanten Einsatz von Platin auf den Nachweis einer BRCA-Mutation zu beschränken. Die BRCA-Mutation ist kein Prädiktor für den Einsatz von Platin. Die BRCA-Mutation erhöht die Chemotherapie-Sensitivität des Tumors, nicht aber speziell jene auf Platin [19].
Chemotherapie bei kleinem TNBC (pT1apN0)?
Auch bei einer Patientin mit kleinem unifokalem TNBC ohne Lymphknotenbefall (< 6 mm, N0) kann eine Chemotherapie-Indikation bestehen, so das Mehrheitsvotum (65,3%) der Panelisten. Die deutsche Expertengruppe meint, dass dies eine Einzelfallentscheidung ist: Eine Chemotherapie-Indikation kann in dieser Situation primär für junge Patientinnen, bei hoch proliferierendem Karzinom oder für Patientinnen mit hohem Sicherheitsbedürfnis (Patientenwunsch) eine Option sein.
HER2+ Mammakarzinom im Fokus
Eine hohe Übereinstimmung zwischen den Panelisten und der deutschen Expertengruppe zeigt sich bei den Abstimmungsergebnissen zur anti-HER2-gerichteten Behandlung beim HER2+ frühen Mammakarzinom:
-
Patientinnen mit HER2+ Mammakarzinom erhalten zusätzlich zur Chemotherapie eine anti-HER2-gerichtete Therapie. Das gilt ab dem Stadium I [2], ist aber kein Standard bei T1a-Karzinomen ohne Lymphknotenbefall (N0) (Mehrheitsvotum (55,3%).
-
Im Stadium I ist der zusätzliche Einsatz von Trastuzumab zur Chemotherapie unabhängig vom ER-Status Standard (Mehrheitsvotum: 61,7%). Das bevorzugte adjuvante Regime ist hier die Kombination Taxan/Trastuzumab (Mehrheitsvotum: 73,5%).
-
Besteht beim HER2+/ER+ Mammakarzinom im Stadium I eine neoadjuvante Trastuzumab-Indikation, impliziert dies nicht, dass der zusätzliche Einsatz von Pertuzumab Standard ist (Mehrheitsvotum: 52,1%, 14,6% Enthaltungen).
-
Eine Pertuzumab-Indikation besteht laut Zulassung im Stadium I bei Patientinnen mit Lymphknotenbefall (N+) und/oder bei negativem ER-Status (ER−) und wird von der AGO Kommission Mamma auch so empfohlen [2]. Das Mehrheitsvotum (48,9%) der St.-Gallen-Panelisten, dass im Stadium I des HER2+ Mammakarzinoms keine Indikation für die doppelte Antikörper-Blockade mit Pertuzumab besteht, widerspricht der AGO-Empfehlung [2].
-
Patientinnen im Stadium II mit Lymphknotenbefall (N+) oder jene im Stadium III sollten (neo)adjuvant vorzugsweise eine Kombinationstherapie mit AC (Doxorubicin/Cyclophosphamid) oder EC (Epirubicin/Cyclophosphamid) gefolgt von einem Taxan plus doppelte Antikörper-Blockade (Trastuzumab/Pertuzumab) erhalten (Mehrheitsvotum: 75,5%).
-
Laut Mehrheitsvotum (76,6%) ist die duale Antikörper-Blockade mit Trastuzumab/Pertuzumab für alle Patientinnen im Stadium II (N+) oder im Stadium 3 die präferierte Therapieoption.
-
Besteht eine Trastuzumab-Indikation, so beträgt die Therapiedauer 12 Monate (Mehrheitsvotum: 89,8%).
Einsatz von Neratinib
Nach (neo)adjuvanter Trastuzumab-Gabe ist der adjuvante Einsatz von Neratinib eine Therapieoption beim HER2+ Mammakarzinom. In der Zulassungsstudie ExteNET [21] profitierte allerdings eine sehr selektionierte Patientengruppe von Neratinib – jene mit HER2+/ER+ Mammakarzinom und mindestens 4 befallenen Lymphknoten. Aufgrund einer nicht unerheblichen Toxizität wird der adjuvante Einsatz von Neratinib kritisch gesehen. Das Abstimmungsergebnis der St.-Gallen-Panelisten ergab eine Befürwortung von Neratinib bei allen nodal-positiven Patientinnen mit HR+/HER2+ Mammakarzinom von 21% der Panelisten und von 27% ab 4 befallenen Lymphknoten bei 29,2% Enthaltungen.
Die deutsche Expertengruppe schließt sich dem Mehrheitsvotum an, verweist aber auf die nicht unerhebliche Toxizität (Diarrhö). In den aktuellen AGO-Empfehlungen der Kommission Mamma erhielt Neratinib aufgrund der ExteNET-Studie [21] eine Plus-/Minus-Bewertung und ist damit eine Option für den Einzelfall [2]. Keine Daten und damit auch keine Indikation besteht für den adjuvanten Einsatz von Neratinib nach dualer Antikörper-Blockade.
Tumorrest nach neoadjuvanter Systemtherapie
Die St.-Gallen-Panelisten und die deutsche Expertengruppe sind sich einig, dass die neoadjuvante systemische Therapie das bevorzugte Behandlungskonzept für Patientinnen mit TNBC und HER2+ Mammakarzinom im Stadium II/III ist – unabhängig davon, ob eine brusterhaltende Operation durchführbar ist oder nicht (Mehrheitsvotum: 98,0%). Der entscheidende Vorteil des neoadjuvanten Konzepts ist die Überprüfung des Ansprechens [2].
Bleibt bei Patientinnen mit TNBC nach neoadjuvanter Sequenztherapie mit AC-Taxan ein Tumorrest, stimmt die deutsche Expertengruppe dem Mehrheitsvotum der St.-Gallen-Panelisten zu, diese Patientinnen adjuvant mit Capecitabin weiter zu behandeln [22], [23]. Diese Empfehlung gilt unabhängig von der Größe des Tumorrests (≥/<1 cm) und dem Lymphknotenbefall (N+/N0).
Für Patientinnen mit HER2+ Mammakarzinom und Resttumor in Brust und/oder Axilla nach neoadjuvanter systemischer Therapie ist der postneoadjuvante Einsatz von T-DM1 eine neue Option [24]. Über 90% der St.-Gallen-Panelisten und die deutsche Expertengruppe stimmen zu. Unerheblich ist für den Einsatz von T-DM1 die Größe des Tumorrests bzw. der Tumorlast in der Axilla. Unerheblich ist auch, ob die Patientinnen neoadjuvant Trastuzumab oder die duale Antikörper-Blockade mit Trastuzumab/Pertuzumab zusätzlich zur Chemotherapie erhalten haben.
pCR nach neoadjuvanter Systemtherapie
Ein Diskussionspunkt ist die adjuvante Weiterbehandlung von Patientinnen mit HER2+ Mammakarzinom und pCR nach neoadjuvanter Therapie. Erreichen Patientinnen mit Lymphknotenbefall bei Erstdiagnose unter neoadjuvanter Poly-Chemotherapie und dualer Antikörper-Blockade (Trastuzumab/Pertuzumab) eine pCR, bevorzugt eine einfache Mehrheit (47,7%) der St.-Gallen-Panelisten, adjuvant mit beiden Antikörpern weiter zu behandeln; 38,6% würden adjuvant nur Trastuzumab einsetzen. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum zu. Dies, so die Begründung der deutschen Experten, ist zwar nicht durch Studien belegt, aber als Rationale wird die Tumorbiologie herangezogen. Diese verändert sich nicht durch die pCR, weshalb ein erhöhtes Risiko bleibt, das den Einsatz beider Antikörper begründet.
Das gilt aus deutscher Sicht auch für Patientinnen ohne Lymphknotenbefall (cN0) bei Erstdiagnose, wenn zusätzlich zur neoadjuvanten Poly-Chemotherapie beide Antikörper eingesetzt wurden (laut Zulassung bei HER2+/ER−). Die St.-Gallen-Panelisten hatten in diesem Fall mehrheitlich (52,2%) für die adjuvante Weiterbehandlung mit Trastuzumab gestimmt. Aus deutscher Sicht sollte nicht deeskaliert werden, wenn ein erhöhtes Ausgangsrisiko (z. B. ER−) besteht.
Adjuvante „bone modifying“-Therapie
Der zusätzliche adjuvante Einsatz eines Bisphosphonats (Zoledronsäure alle 6 Monate oder orales Clodronat täglich) zur adjuvanten endokrinen Therapie kann bei postmenopausalen Patientinnen die krankheitsfreie Zeit (DFS) verlängern und das Gesamtüberleben verbessern. Das gilt unabhängig von der Knochendichte der betroffenen Frau. In einer Metaanalyse [25] zum adjuvanten Einsatz der Bisphosphonate haben allerdings nur die Patientinnen mit Lymphknotenbefall von einer Bisphosphonattherapie profitiert. Die österreichische ABCSG 12-Studie [26] zeigt, dass das auch für prämenopausale Patientinnen gilt, wenn diese im Rahmen der adjuvanten endokrinen Therapie zusätzlich ein GnRH-Analogon erhalten.
Vor dem Hintergrund dieser Daten sprach sich eine knappe Mehrheit (53,1%) der Panelisten dafür aus, bei prämenopausalen Patientinnen, die adjuvant ein GnRH-Analogon plus Tamoxifen oder AI erhalten, zusätzlich ein Bisphosphonat (Zoledronsäure oder Clodronat), zu empfehlen, um unabhängig von der Knochendichte das DFS zu verlängern.
Die deutsche Expertengruppe war sich bei dieser Frage nicht einig. Kritiker wenden ein, dass die Indikation des Bisphosphonats zur DFS-Verlängerung bei prämenopausalen Patientinnen nur auf einer Studie (ABCSG-12) [26] beruht. Die AGO Mamma hat entsprechend eine „Plus/Minus“-Bewertung (Einzelfallentscheidung) vergeben [2]. Einigkeit besteht, dass der osteoprotektive Effekt der Bisphosphonate unabhängig von der Indikation der DFS-Verlängerung zu sehen ist.
Bei postmenopausalen Patientinnen stimmten die deutschen Experten den St.-Gallen-Panelisten (83,7%) zu, dass ein Bisphosphonat zur DFS-Verlängerung eingesetzt werden kann. Interessanterweise gaben aber nur 42,6% der Panelisten in einer zusätzlichen Abstimmung an, dies in der eigenen klinischen Praxis umzusetzen. Keine Indikation mit Blick auf das DFS besteht aufgrund der kontroversen Datenlage für den adjuvanten Einsatz von Denosumab (60 mg, alle 6 Monate). Die deutsche Expertengruppe stimmt hier dem Mehrheitsvotum (75%) der Panelisten zu. Die Zulassungsstudie (D-CARE) [27] konnte im Gegensatz zur ABCSG-18-Studie [28], [29] keine Verbesserung der Heilungschance unter Denosumab belegen. Allerdings wurde auch in der D-Care-Studie ein positiver Einfluss der Substanz auf die Frakturrate gesehen [27].
Fertilitätserhalt
Ein Fertilitätserhalt unter (neo)adjuvanter Chemotherapie mittels Suppression der Ovarfunktion sollte unabhängig vom Hormonrezeptor-(HR-)Status des Tumors allen Patientinnen mit Kinderwunsch angeboten werden [2]. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum der Panelisten sowohl für Patientinnen mit HR-negativem (91,5%) als auch HR-positivem Karzinom (79,6%) zu und ergänzt, dass dies für alle Patientinnen im gebärfähigen Alter gilt. Die deutschen Experten verweisen für weitere Informationen auf die AGO-Empfehlung ([Abb. 7]) und die Initiative FertiPROTEKT (www.fertiprotekt.de).


Genetische Testung auf Hochrisiko-Mutationen?
Eine genetische Testung auf Hochrisiko-Mutationen (z. B. BRCA1/2-Testung) setzt eine entsprechende Aufklärung und Beratung der Patientin voraus. Die deutsche Expertengruppe stimmt dem Mehrheitsvotum (70,8%) der St.-Gallen-Panelisten zu, dass eine solche Testung nicht für alle Patientinnen – unabhängig vom familiären Risiko – in Betracht zu ziehen ist. Einstimmig (100%!) votierten die Panelisten dafür, bei Frauen aus Hochrisiko-Familien (eindeutig positive Familienanamnese) eine genetische Testung zu empfehlen. Fast einstimmig (95,9%) votierten die Panelisten für die genetische Testung bei Patientinnen, die zum Diagnosezeitpunkt jünger als 35 Jahre alt sind.
Einigkeit besteht, dass ein Alters-Cut-off-Wert von unter 50 Jahren nicht geeignet ist, eine genetische Testung ohne Familienanamnese zu empfehlen. Eine generelle Indikation für eine Testung bei Patientinnen unter 50 Jahre besteht daher nicht. Anders ist das bei Patientinnen mit TNBC. Hier empfehlen die St.-Gallen-Panelisten (85,4%) und die deutschen Experten eine genetische Testung, wenn die Patientin bei Erstdiagnose jünger als 60 Jahre alt ist.
Schwangerschaft nach Brustkrebs
Brustkrebspatientinnen mit Kinderwunsch sollten aktiv beraten werden. Die endokrine Behandlung kann bei Kinderwunsch unterbrochen werden, wenn keine „high-risk“-Situation vorliegt. Dies sollte frühestens nach 18 Monaten geschehen (78,0%). Die deutsche Expertengruppe stimmt daher dem Mehrheitsvotum (79,2%) der Panelisten zu, die Therapie nicht zu einem beliebigen Zeitpunkt abzubrechen. Da der Benefit der adjuvanten endokrinen Therapie mit der Therapiedauer korreliert, favorisieren die deutschen Experten eine endokrine Therapiedauer von mindestens 24 Monaten, bevor eine Schwangerschaft eintritt.
Knapp 60% (59,6%) der St.-Gallen-Panelisten empfehlen, dass sich die Patientin vor der Schwangerschaft einem Re-Staging unterzieht. Die deutsche Expertengruppe findet ein Re-Staging ebenfalls empfehlenswert und ergänzt, dass der Kinderwunsch eine individuelle Entscheidung der Patientin ist. Der behandelnde Arzt sollte die Patientin aufklären sowie konstruktiv und empathisch unterstützen.
Ernährung und Bewegung
Einigkeit besteht, dass Patientinnen auf die insgesamt prognostische Bedeutung eines gesunden Lebensstils mit beispielsweise abwechslungsreicher (gesunder) Ernährung und angemessener sportlicher Aktivität mit dem Ziel, deutliches Übergewicht zu vermeiden, hingewiesen werden sollten.
Duktales Carcinoma in situ (DCIS)
Die im Rahmen des St.-Gallen-Konsensus-Meetings gestellten Abstimmungsfragen zur Behandlung des DCIS geben aus deutscher Sicht die Komplexität der Situation nicht ausreichend wieder. Vor diesem Hintergrund stimmt die deutsche Expertengruppe den St.-Gallen-Panelisten (97,9%) zu, dass Patientinnen mit einem kleinen DCIS eine günstigere Prognose haben und eine weniger intensive Behandlung benötigen. Das gilt insbesondere dann, wenn das DCIS im Rahmen des Screenings entdeckt wird, die Patientin ≥ 50 Jahre alt ist und das DCIS eine günstige Biologie aufweist, die für ein niedriges Risiko steht.
Bei günstigen prognostischen Faktoren und einem freien Schnittrand (≥ 5 mm) kann laut Votum der Panelisten (84,4%) auf eine adjuvante Bestrahlung des DCIS verzichtet werden. Die Frage, ob auf eine adjuvante endokrine Behandlung verzichtet werden kann, bejahte eine knappe Mehrheit (55,6%) der Panelisten für alle DCIS-Patientinnen und 42,2% nur für DCIS-Patientinnen mit günstigen prognostischen Faktoren. Bei günstigen prognostischen Faktoren würden 66,7% der Panelisten sowohl auf die adjuvante Bestrahlung als auch auf die adjuvante endokrine Therapie verzichten.
Die deutsche Expertengruppe ergänzt, dass der Einsatz von Tamoxifen vor allem eine präventive Maßnahme ist mit dem Ziel, ipsi- oder kontralaterale Zweitkarzinome zu verhindern. Die Entscheidung, eine Patientin mit DCIS adjuvant zu behandeln, erfordert eine individuelle Abwägung von Nutzen und Risiko und entscheidet sich anhand vieler Faktoren, wie z. B. der Tumorgröße oder auch dem Alter der Patientin. Bislang ist für DCIS-Patientinnen weder durch die endokrine Therapie noch die Strahlentherapie ein Überlebensvorteil beschrieben. Der Sicherheitsabstand von ≥ 5 mm in den Fragestellungen ist aus deutscher Sicht arbiträr, da derzeit beim DCIS kein exakter Sicherheitsabstand definiert ist.
Magnitude of absolute Benefit
Bei der letzten Abstimmung der St.-Gallen-Panelisten schloss sich der Kreis zum Motto der diesjährigen Konsensus-Konferenz: Über 90% der Panelisten stimmten zu, dass zur umfassenden Aufklärung einer Brustkrebspatientin gehört, dass sie über die Möglichkeiten und Grenzen der jeweiligen therapeutischen Maßnahmen informiert wird. Bei Therapieoptionen mit nur sehr begrenzten Erfolgsaussichten sollte dies ehrlich kommuniziert und auch über die Option gesprochen werden, auf die Behandlung zu verzichten. Die deutsche Expertengruppe stimmt zu.
Anmerkung
Das Post-St.-Gallen-Treffen wurde von der Firma Aurikamed Institute GmbH organisiert und durchgeführt und durch einen inhaltlich nicht einschränkenden Grant der Firma Celgene GmbH ermöglicht. Die Verantwortung für die Manuskripterstellung lag ausschließlich bei den Autoren. Für die redaktionelle Unterstützung bei der Erstellung des Manuskriptes danken die Autoren Frau Birgit-Kristin Pohlmann, Nordkirchen.
Conflict of Interest/Interessenkonflikt
Prof. Michael Untch: Honoraria to the employer (for AdBoard participation, lectures) as well as travel support from Amgen, AstraZeneca, BMS, Celgene, Daiichi Sankyo, Eisai, Janssen Cilag, Johnson & Johnson, Lilly Deutschland, Lilly International, MSD, Mundipharma, Myriad Genetics, Odonate, Pfizer, Puma Biotechnology, Riemser, Roche, Sanofi Aventis, Sividon Diagnostics, TEVA Pharmaceuticals Ind. Ltd. Prof. Christoph Thomssen received honoraria from AstraZeneca, Celgene, Genomic Health, Novartis, NanoString, Pfizer, Roche and research support from NanoString. Dr. med. Ingo Bauerfeind has no conflict of interest. Prof. Michael Braun received honoraria from AstraZeneca, Celgene, Daiichi Sankyo, Genomic Health, Eisai, Genomic Health, GlaxoSmithKline, Medac, Novartis, Pfizer, PumaBiotechnology, Roche, Teva. Prof. Sara Brucker received honoraria from Novartis, Pfizer, AstraZeneca, Roche and research support from Genomic Health. Prof. Ricardo Felberbaum has no conflict of interest. Dr. med. Friederike Hagemann has no conflict of interest. Renate Haidinger has no conflict of interest. Prof. Arnd Hönig received honoraria from Amgen, Astra Zeneca, Celgene, MSD, Pfizer, Roche, Novartis, as well as research support from Roche and Genentech and travel grants from Roche, AstraZeneca, Daiichi Sankyo, Pfizer. Prof. Jens Huober received honoraria from Celgene, Roche, Novartis, Hexal, Pfizer, AstraZeneca, Lilly, Amgen, Eisai as well as research support from Celgene, Hexal, Novartis and travel grant from Roche, Novartis and Celgene. Prof. Christian Jackisch received honoraria from Celgene, Novartis, Pfizer, AstraZeneca, Roche and research support from Genomic Health. Prof. Thorsten Kühn has no conflict of interest. PD Dr. Hans-Christian Kolberg received honoraria from Pfizer, Novartis, Roche, Genomic Health, Amgen, AstraZeneca, Riemser, Carl Zeiss Meditec, TEVA, Theraclion, Janssen-Cilag, GSK, LIV Pharma as well as honoraria for consultancy work from Pfizer, Novartis, SurgVision, Carl Zeiss Meditec, Amgen, Onkowissen and owns shares of Theraclion SA, Phaon Scientific GmbH. Travel grant from Carl Zeiss Meditec, LIV Pharam, Novartis, Amgen, Pfizer and Daiichi Sankyo. Prof. Cornelia Kolberg-Liedtke received honoraria from Roche, AstraZeneca, Celgene, Novartis, Pfizer, Lilly, Hexal, Amgen, Eisai, SonoScape as well as honoraria for consultancy work from Phaon Scientific, Novartis, Pfizer, Celgene as well as research support from Roche, Novartis, Pfizer. Travel grant from Novartis and Roche. Prof. Diana Lüftner received honoraria from AstraZeneca, Celgene, Pfizer, Novartis, Amgen, Roche, Loreal, Teva, Tesaro and Eli Lilly. Prof. Nicolai Maass received honoraria from Amgen, AstraZeneca, Celgene, Lilly, MSD, Pfizer, Roche, Novartis, Daiichi Sankyo. Prof. Toralf Reimer received honoraria from Novartis, Pfizer, Lilly, Celgene and AstraZeneca. Prof. Andreas Schneeweiss received honoraria from Celgene, Roche, Pfizer, AstraZeneca, Novartis, MSD, Tesaro, Lilly as well as research support from Celgene, Roche, AbbVie, Molecular Partner as well as travel grants from Celgene, Roche and Pfizer. Eva Schumacher-Wulff has no conflict of interest. Prof. Florian Schütz received honoraria for lectures and consultations from Amgen, AstraZeneca, ClinSol, MSD, Novartis, Pfizer, Riemser, Roche as well as a travel grant from AstraZeneca, Pfizer and Roche. PD Dr. Marc Thill received honoraria from Amgen, AstraZeneca, Aurikamed, BiomʼUp, Celgene, Daiichi Sankyo, Eisai, Genomic Health, Hexal, Lilly, MCI, Medtronic, MSD, Myriad, Neodynamics, Norgine, Novartis, OnkoLive, OmniaMed, pfm Medical, Pfizer, Roche, Tesaro, Teva, RTI Surgical, and research support from Genomic Health. Dr. med. Rachel Wuerstlein received honoraria from Agendia, Amgen, AstraZeneca, Boehringer Ingelheim, Carl Zeiss, Celgene, Daiichi-Sankyo, Esai, Genomic Health, GSK, Lilly, MSD, Mundipharma, Nanostring, Novartis, Odonate, Paxman, Palleos, Pfizer, Pierre Fabre, PumaBiotechnology, Riemser, Roche, Sandoz/Hexal, Seattle Genetics, Tesaro Bio, Teva. Prof. Peter A. Fasching reports grants from Novartis, Cepheid and Biontech as well as personal contributions from Novartis, Roche, Pfizer, Celgene, Daiichi-Sankyo, Teva, AstraZeneca, MSD, Myelo Therapeutics, Macrogenics, Eisai and Puma. Prof. Nadia Harbeck received honoraria from Agendia, Amgen, Celgene, Genomic Health, Lilly, MSD, Nanostring, Novartis, Pfizer, Roche, Sandoz.
Prof. Michael Untch: Honoraria an den Arbeitgeber (für AdBoard-Teilnahme, Vorträge) sowie Reiseunterstützung von Amgen, AstraZeneca, BMS, Celgene, Daiichi Sankyo, Eisai, Janssen Cilag, Johnson & Johnson, Lilly Deutschland, Lilly International, MSD, Mundipharma, Myriad Genetics, Odonate, Pfizer, Puma Biotechnology, Riemser, Roche, Sanofi Aventis, Sividon Diagnostics, Teva Pharmaceuticals Ind. Ltd. Prof. Christoph Thomssen erhielt Honoraria von AstraZeneca, Celgene, Genomic Health, Novartis, NanoString, Pfizer, Roche und Forschungsunterstützung von NanoString. Dr. med. Ingo Bauerfeind hat keinen Interessenkonflikt. Prof. Michael Braun erhielt Honoraria von AstraZeneca, Celgene, Daiichi Sankyo, Genomic Health, Eisai, Genomic Health, GlaxoSmithKline, Medac, Novartis, Pfizer, Puma Biotechnology, Roche, Teva. Prof. Sara Brucker erhielt Honoraria von Novartis, Pfizer, AstraZeneca, Roche und Forschungsunterstützung von Genomic Health. Prof. Ricardo Felberbaum hat keinen Interessenkonflikt. Dr. med. Friederike Hagemann hat keinen Interessenkonflikt. Renate Haidinger hat keinen Interessenkonflikt. Prof. Arnd Hönig erhielt Honoraria von Amgen, AstraZeneca, Celgene, MSD, Pfizer, Roche, Novartis, sowie Forschungsunterstützung von Roche und Genentech und Reiseunterstützung von Roche, AstraZeneca, Daiichi Sankyo, Pfizer. Prof. Jens Huober erhielt Honoraria von Celgene, Roche, Novartis, Hexal, Pfizer, AstraZeneca, Lilly, Amgen, Eisai sowie Forschungsunterstützung von Celgene, Hexal, Novartis und Reiseunterstützung von Roche, Novartis und Celgene. Prof. Christian Jackisch erhielt Honoraria von Celgene, Novartis, Pfizer, AstraZeneca, Roche und Forschungsunterstützung von Genomic Health. Prof. Thorsten Kühn hat keinen Interessenkonflikt. PD Dr. Hans-Christian Kolberg erhielt Honoraria von Pfizer, Novartis, Roche, Genomic Health, Amgen, AstraZeneca, Riemser, Carl Zeiss Meditec, Teva, Theraclion, Janssen-Cilag, GlaxoSmithKline, LIV Pharma sowie Honorare für Beratertätigkeit von Pfizer, Novartis, SurgVision, Carl Zeiss Meditec, Amgen, Onkowissen und hat Aktien von Theraclion SA, Phaon Scientific GmbH. Reiseunterstützung von Carl Zeiss Meditec, LIV Pharma, Novartis, Amgen, Pfizer und Daiichi Sankyo. Prof. Cornelia Kolberg-Liedtke erhielt Honoraria von Roche, AstraZeneca, Celgene, Novartis, Pfizer, Lilly, Hexal, Amgen, Eisai, SonoScape sowie Honorare für Beratertätigkeit von Phaon Scientific, Novartis, Pfizer, Celgene sowie Forschungsunterstützung von Roche, Novartis, Pfizer. Reiseunterstützung von Novartis und Roche. Prof. Diana Lüftner erhielt Honoraria von AstraZeneca, Celgene, Pfizer, Novartis, Amgen, Roche, Loreal, Teva, Tesaro und Eli Lilly. Prof. Nicolai Maass erhielt Honoraria von Amgen, AstraZeneca, Celgene, Lilly, MSD, Pfizer, Roche, Novartis und Daiichi Sankyo. Prof. Toralf Reimer erhielt Honoraria von Novartis, Pfizer, Lilly, Celgene und AstraZeneca. Prof. Andreas Schneeweiss erhielt Honoraria von Celgene, Roche, Pfizer, AstraZeneca, Novartis, MSD, Tesaro, Lilly sowie Forschungsunterstützung von Celgene, Roche, AbbVie, Molecular Partner sowie Reiseunterstützung von Celgene, Roche und Pfizer. Eva Schumacher-Wulff hat keinen Interessenkonflikt. Prof. Florian Schütz erhielt Honoraria für Vorträge und Beratungen von Amgen, AstraZeneca, ClinSol, MSD, Novartis, Pfizer, Riemser, Roche sowie Reiseunterstützung von AstraZeneca, Pfizer und Roche. PD Dr. Marc Thill erhielt Honoraria von Amgen, AstraZeneca, Aurikamed, BiomʼUp, Celgene, Daiichi Sankyo, Eisai, Genomic Health, Hexal, Lilly, MCI, Medtronic, MSD, Myriad, Neodynamics, Norgine, Novartis, OnkoLive, OmniaMed, pfm Medical, Pfizer, Roche, Tesaro, Teva, RTI Surgical und Forschungsunterstützung von Genomic Health. Dr. med. Rachel Wuerstlein erhielt Honoraria von Agendia, Amgen, AstraZeneca, Boehringer Ingelheim, Carl Zeiss, Celgene, Daiichi-Sankyo, Esai, Genomic Health, GSK, Lilly, MSD, Mundipharma, Nanostring, Novartis, Odonate, Paxman, Palleos, Pfizer, Pierre Fabre, PumaBiotechnology, Riemser, Roche, Sandoz/Hexal, Seattle Genetics, Tesaro Bio, Teva. Prof. Peter A. Fasching berichtet über Zuschüsse von Novartis, Cepheid und Biontech sowie persönliche Zuwendungen von Novartis, Roche, Pfizer, Celgene, Daiichi-Sankyo, Teva, AstraZeneca, MSD, Myelo Therapeutics, Macrogenics, Eisai und Puma. Prof. Nadia Harbeck erhielt Honoraria von Agendia, Amgen, Celgene, Genomic Health, Lilly, MSD, Nanostring, Novartis, Pfizer, Roche, Sandoz.
* Writing Committee
** Steering Committee
# St. Gallen Panel Expert
-
References/Literatur
- 1 Kolberg H-C, Schneeweiss A, Fehm TN. et al. Update Breast Cancer 2019 Part 3 – Current Developments in Early Breast Cancer: Review and Critical Assessment by an International Expert Panel. Geburtsh Frauenheilk 2019; 79: 470-482
- 2 Ditsch N, Untch M, Thill M. et al. AGO Recommendations for the Diagnosis and Treatment of Patients with Early Breast Cancer: Update 2019. Breast Care 2019; 14 im Druck. Online: http://www.ago-online.de last access: 25.05.2019
- 3 Reimer T, Stachs A, Nekljudova V. et al. Restricted Axillary Staging in Clinically and Sonographically Node-Negative Early Invasive Breast Cancer (c/iT1-1) in the Context of Breast Conserving Therapy: First Results Following Commencement of the Intergroup-Sentinel-Mamma (INSEMA) Trial. Geburtsh Frauenheilk 2017; 77: 149-157
- 4 Gentilini O, Veronesi U. Abandoning sentinel lymph node biopsy in early breast cancer? A new trial in progress at the European Institute of Oncology of Milan (SOUND: Sentinel node vs Observation after axillary UltraSouND). Breast 2012; 21: 678-681
- 5 Giuliano AE, Ballman KV, McCall L. et al. Effect of Axillary Dissection vs. No Axillary Dissection on 10-Year Overall Survival Among Women With Invasive Breast Cancer and Sentinel Node Metastasis: The ACOSOG Z0011 (Alliance) Randomized Clinical Trial. JAMA 2017; 318: 918-926
- 6 Donker M, van Tienhoven G, Straver ME. et al. Radiotherapy or surgery of the axilla after a positive sentinel node in breast cancer (EORTC 10981-22023 AMAROS): a randomised, multicentre, open-label, phase 3 non-inferiority trial. Lancet Oncol 2014; 15: 1303-1310
- 7 Online: http://www.astro.org last access: 27.03.2019
- 8 Smith BD, Arthur DW, Buchholz TA. et al. Consensus Statement der ASTRO. Int J Rad Oncol Bio Phys 2009; 74: 987-1001
- 9 Online: http://www.estro.org last access: 27.03.2019
- 10 Polgàr C, Van Limbergen E, Pötter R. et al. Patient selection for accelerated partial-breast irradiation (APBI) after breast-conserving surgery: recommendations of the Groupe Européen de Curiethérapie-European Society for Therapeutic Radiology and Oncology (GEC-ESTRO) breast cancer working group based on clinical evidence (2009). Radiother Oncol 2010; 94: 264-273
- 11 Schmid P, Adams S, Rugo HS. et al. Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. N Engl J Med 2018;
- 12 Emens LA, Loi S, Rugo HS. et al. Impassion130: Efficacy in immune biomarker subgroups from the global, randomized, double-blind, placebo-controlled, Phase III study of Atezolizumab + nab-paclitaxel in patients with treatment-naïve, locally advanced or metastatic triple-negative breast cancer. SABCS 2018; abstract/oral presentation GS1-04.
- 13 Pagani O, Regan MM. Francis PA; TEXT and SOFT Investigators, International Breast Cancer Study Group. Exemestane with ovarian suppression in premenopausal breast cancer. N Engl J Med 2014; 371: 1358-1359
- 14 Sparano JA, Gray RJ, Makower DF. et al. Prospective Validation of 21-Gene Expression Assay in Breast Cancer. N Engl J Med 2015; 373: 2005-2014
- 15 Cardoso F, vanʼt Veer LJ, Bogaerts J. et al. 70-Gene Signature as an Aid to Treatment Decisions in Early-Stage Breast Cancer. N Engl J Med 2016; 375: 717-729
- 16 Gluz O, Nitz UA, Christgen M. et al. West German Study Group Phase III Plan B Trial: First Prospective Outcome Data for the 21-Gene Recurrence Score Assay and Concordance of Prognostic markers by Central and Local Pathology Assessment. J Clin Oncol 2016; 24: 2341-2349
- 17 Loibl S, OʼShaughnessy J, Untch M. et al. Addition of the PARP inhibitor veliparib plus carboplatin or carboplatin alone to standard neoadjuvant chemotherapy in triple-negative breast cancer (BrighTNess). A randomised, phase 3 trial. Lancet Oncol 2018; 19: 497-509
- 18 Sparano JA, Zhao F, Martino S. et al. Long-Term Follow-Up of the E1199 Phase III Trial Evaluating the Role of Taxane and Schedule in Operable Breast Cancer. J Clin Oncol 2015; 33: 2353-2360
- 19 Hahnen E, Lederer B, Hauke J. et al. Germline Mutation Status, Pathological Complete Response, and Disease-free Survival in Triple-Negative Breast Cancer: Secondary Analysis of the GeparSixto Randomized Clinical Trial. JAMA Oncol 2017; 3: 1378-1385
- 20 Petrelli F. The value of platinum agents as neoadjuvant chemotherapy in triple-negative breast cancers: a systematic review and meta-analysis. Breast Cancer Res Treat 2014; 144: 223
- 21 Martin M, Holmes FA, Ejlertsen B. et al. Neratinib after trastuzumab-based adjuvant therapy in HER2-positive breast cancer (ExteNET): 5-year analysis of a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2017;
- 22 Masuda N, Lee S-J, Ohtani S. et al. Adjuvant Capecitabine for Breast Cancer after Preoperative Chemotherapy. N Engl J Med 2017; 376: 2147-2156
- 23 Zujewski JA, Rubinstein L. CREATE-X a role for capecitabine in early-stage breast cancer: an analysis of available data. NPJ Breast Cancer 2017; 3: 27
- 24 von Minckwitz G, Huang CS, Mano MS. et al. Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer. N Engl J Med 2018;
- 25 Early Breast Cancer Trialistsʼ Collaborative Group (EBCTCG). Adjuvant bisphosphonate treatment in early breast cancer: meta-analyses of individual patient data from randomised trials. Lancet 2015; 386: 1353
- 26 Gnant M, Mlineritsch B, Stoeger H. et al. Adjuvant endocrine therapy plus zoledronic acid in premenopausal women with early-stage breast cancer: 62-month follow-up from the ABCSG-12 randomised trial. Lancet Oncol 2011; 12: 631-641
- 27 Coleman RE, Finkelstein D, Barrios CH. et al. Adjuvant denosumab in early breast cancer: First results from international multicenter randomized phase III placebo controlled D-CARE study. J Clin Oncol 2018; 36 (Suppl.) 501
- 28 Gnant M, Pfeiler G, Steger GG. et al. Adjuvant denosumab in early breast cancer: Disease-free survival analysis of 3,425 postmenopausal patients in the ABCSG-18 trial. J Clin Oncol 2018; 36 (no. 15_suppl): 500 doi:10.1200/JCO.2018.36.15_suppl.500
- 29 Gnant M, Pfeiler G, Dubsky PC. et al. Adjuvant denosumab in breast cancer (ABCSG-18): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet 2015; 386: 433-443
Correspondence/Korrespondenzadresse
-
References/Literatur
- 1 Kolberg H-C, Schneeweiss A, Fehm TN. et al. Update Breast Cancer 2019 Part 3 – Current Developments in Early Breast Cancer: Review and Critical Assessment by an International Expert Panel. Geburtsh Frauenheilk 2019; 79: 470-482
- 2 Ditsch N, Untch M, Thill M. et al. AGO Recommendations for the Diagnosis and Treatment of Patients with Early Breast Cancer: Update 2019. Breast Care 2019; 14 im Druck. Online: http://www.ago-online.de last access: 25.05.2019
- 3 Reimer T, Stachs A, Nekljudova V. et al. Restricted Axillary Staging in Clinically and Sonographically Node-Negative Early Invasive Breast Cancer (c/iT1-1) in the Context of Breast Conserving Therapy: First Results Following Commencement of the Intergroup-Sentinel-Mamma (INSEMA) Trial. Geburtsh Frauenheilk 2017; 77: 149-157
- 4 Gentilini O, Veronesi U. Abandoning sentinel lymph node biopsy in early breast cancer? A new trial in progress at the European Institute of Oncology of Milan (SOUND: Sentinel node vs Observation after axillary UltraSouND). Breast 2012; 21: 678-681
- 5 Giuliano AE, Ballman KV, McCall L. et al. Effect of Axillary Dissection vs. No Axillary Dissection on 10-Year Overall Survival Among Women With Invasive Breast Cancer and Sentinel Node Metastasis: The ACOSOG Z0011 (Alliance) Randomized Clinical Trial. JAMA 2017; 318: 918-926
- 6 Donker M, van Tienhoven G, Straver ME. et al. Radiotherapy or surgery of the axilla after a positive sentinel node in breast cancer (EORTC 10981-22023 AMAROS): a randomised, multicentre, open-label, phase 3 non-inferiority trial. Lancet Oncol 2014; 15: 1303-1310
- 7 Online: http://www.astro.org last access: 27.03.2019
- 8 Smith BD, Arthur DW, Buchholz TA. et al. Consensus Statement der ASTRO. Int J Rad Oncol Bio Phys 2009; 74: 987-1001
- 9 Online: http://www.estro.org last access: 27.03.2019
- 10 Polgàr C, Van Limbergen E, Pötter R. et al. Patient selection for accelerated partial-breast irradiation (APBI) after breast-conserving surgery: recommendations of the Groupe Européen de Curiethérapie-European Society for Therapeutic Radiology and Oncology (GEC-ESTRO) breast cancer working group based on clinical evidence (2009). Radiother Oncol 2010; 94: 264-273
- 11 Schmid P, Adams S, Rugo HS. et al. Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. N Engl J Med 2018;
- 12 Emens LA, Loi S, Rugo HS. et al. Impassion130: Efficacy in immune biomarker subgroups from the global, randomized, double-blind, placebo-controlled, Phase III study of Atezolizumab + nab-paclitaxel in patients with treatment-naïve, locally advanced or metastatic triple-negative breast cancer. SABCS 2018; abstract/oral presentation GS1-04.
- 13 Pagani O, Regan MM. Francis PA; TEXT and SOFT Investigators, International Breast Cancer Study Group. Exemestane with ovarian suppression in premenopausal breast cancer. N Engl J Med 2014; 371: 1358-1359
- 14 Sparano JA, Gray RJ, Makower DF. et al. Prospective Validation of 21-Gene Expression Assay in Breast Cancer. N Engl J Med 2015; 373: 2005-2014
- 15 Cardoso F, vanʼt Veer LJ, Bogaerts J. et al. 70-Gene Signature as an Aid to Treatment Decisions in Early-Stage Breast Cancer. N Engl J Med 2016; 375: 717-729
- 16 Gluz O, Nitz UA, Christgen M. et al. West German Study Group Phase III Plan B Trial: First Prospective Outcome Data for the 21-Gene Recurrence Score Assay and Concordance of Prognostic markers by Central and Local Pathology Assessment. J Clin Oncol 2016; 24: 2341-2349
- 17 Loibl S, OʼShaughnessy J, Untch M. et al. Addition of the PARP inhibitor veliparib plus carboplatin or carboplatin alone to standard neoadjuvant chemotherapy in triple-negative breast cancer (BrighTNess). A randomised, phase 3 trial. Lancet Oncol 2018; 19: 497-509
- 18 Sparano JA, Zhao F, Martino S. et al. Long-Term Follow-Up of the E1199 Phase III Trial Evaluating the Role of Taxane and Schedule in Operable Breast Cancer. J Clin Oncol 2015; 33: 2353-2360
- 19 Hahnen E, Lederer B, Hauke J. et al. Germline Mutation Status, Pathological Complete Response, and Disease-free Survival in Triple-Negative Breast Cancer: Secondary Analysis of the GeparSixto Randomized Clinical Trial. JAMA Oncol 2017; 3: 1378-1385
- 20 Petrelli F. The value of platinum agents as neoadjuvant chemotherapy in triple-negative breast cancers: a systematic review and meta-analysis. Breast Cancer Res Treat 2014; 144: 223
- 21 Martin M, Holmes FA, Ejlertsen B. et al. Neratinib after trastuzumab-based adjuvant therapy in HER2-positive breast cancer (ExteNET): 5-year analysis of a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2017;
- 22 Masuda N, Lee S-J, Ohtani S. et al. Adjuvant Capecitabine for Breast Cancer after Preoperative Chemotherapy. N Engl J Med 2017; 376: 2147-2156
- 23 Zujewski JA, Rubinstein L. CREATE-X a role for capecitabine in early-stage breast cancer: an analysis of available data. NPJ Breast Cancer 2017; 3: 27
- 24 von Minckwitz G, Huang CS, Mano MS. et al. Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer. N Engl J Med 2018;
- 25 Early Breast Cancer Trialistsʼ Collaborative Group (EBCTCG). Adjuvant bisphosphonate treatment in early breast cancer: meta-analyses of individual patient data from randomised trials. Lancet 2015; 386: 1353
- 26 Gnant M, Mlineritsch B, Stoeger H. et al. Adjuvant endocrine therapy plus zoledronic acid in premenopausal women with early-stage breast cancer: 62-month follow-up from the ABCSG-12 randomised trial. Lancet Oncol 2011; 12: 631-641
- 27 Coleman RE, Finkelstein D, Barrios CH. et al. Adjuvant denosumab in early breast cancer: First results from international multicenter randomized phase III placebo controlled D-CARE study. J Clin Oncol 2018; 36 (Suppl.) 501
- 28 Gnant M, Pfeiler G, Steger GG. et al. Adjuvant denosumab in early breast cancer: Disease-free survival analysis of 3,425 postmenopausal patients in the ABCSG-18 trial. J Clin Oncol 2018; 36 (no. 15_suppl): 500 doi:10.1200/JCO.2018.36.15_suppl.500
- 29 Gnant M, Pfeiler G, Dubsky PC. et al. Adjuvant denosumab in breast cancer (ABCSG-18): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet 2015; 386: 433-443






























