RSS-Feed abonnieren

DOI: 10.1055/a-2111-7394
Toxoplasma-gondii-Infektion in der Schwangerschaft – Empfehlungen der Arbeitsgemeinschaft Geburtshilfe und Pränatalmedizin (AGG – Sektion Maternale Erkrankungen)
Artikel in mehreren Sprachen: English | deutschAutor*innen
Zusammenfassung
Ziel Diese Empfehlungen der AGG (Arbeitsgemeinschaft für Geburtshilfe und Pränatalmedizin, Sektion maternale Erkrankungen) haben das Ziel der Verbesserung der Diagnostik und des Managements von Toxoplasma-gondii-Infektionen in der Schwangerschaft.
Methoden Basierend auf der aktuellen Literatur entwickelten die Mitglieder der Task Force die vorliegenden Empfehlungen und Stellungnahmen. Diese Empfehlungen wurden nach einem Konsens der Mitglieder der Arbeitsgruppe verabschiedet.
Empfehlungen Das folgende Manuskript beschäftigt sich mit der Epidemiologie und Pathophysiologie von Toxoplasma-gondii-Infektionen in der Schwangerschaft und enthält Empfehlungen zu maternaler und fetaler Diagnostik, Transmissionsprophylaxe, Therapie, Prävention, Screening und peripartalem Management.
1 Einleitung
Die Toxoplasma-gondii-Infektion in der Schwangerschaft ist potenziell für den Fetus gefährlich. Da es in Deutschland kein gesetzlich vorgegebenes Screening gibt und keine eindeutige Evidenz zum Vorgehen in der Schwangerschaft vorhanden ist, existiert kein einheitliches Vorgehen in Bezug auf Diagnostik und Therapie. Ziel dieser Empfehlung ist es, die aktuelle Datenlage zu sichten und unter Berücksichtigung der zur Verfügung stehenden Literatur Empfehlungen zum Vorgehen in der Schwangerschaft zu formulieren.
2 Methodik
Grundlage für die Erarbeitung war der RKI-Ratgeber Toxoplasmose aus dem Jahr 2018 [1]. Darüber hinaus führten wir eine Medline-Literaturrecherche unter Verwendung der Suchbegriffe „pregnancy AND toxoplasmosis“ und der Filter „Meta-Analysis“, „systematic review“ und „10 years“ durch. Die Abstracts wurden auf ihre Relevanz geprüft und die entsprechenden Studien für die Publikation verwendet. Zu einzelnen spezifischeren Fragestellungen wurden themenbezogene Literaturrecherchen angeschlossen.
3 Erreger, Übertragung und Epidemiologie
Die Toxoplasmose ist eine Zoonose, die durch das obligat intrazelluläre Protozoon Toxoplasma (T.) gondii verursacht wird.
In Katzen und anderen Feliden (Endwirte) kommt es nach peroraler Aufnahme des Parasiten im Darmepithel zu einer geschlechtlichen Vermehrung des Erregers ([Abb. 1]). Die anschließend über den Kot ausgeschiedenen Oozysten enthalten nach 24 Stunden Reifung an der Luft infektiöse Sporozoiten, die je nach Klimabedingungen mehrere Monate bis Jahre in der Umwelt überleben können.
|
Land |
Autor |
Jahr |
Art der Publikation |
Empfehlungen |
|||
|---|---|---|---|---|---|---|---|
|
Screening |
Behandlung |
AC |
Follow-up |
||||
|
Frankreich |
Mandelbrot et al. [47] |
2021 |
Expertenmeinung |
|
maternale Infektion zwischen 2 und 6 SSW:
maternale Infektion zwischen 6 und 14 SSW:
maternale Infektion zwischen 14 und 32 SSW:
maternale Infektion nach 32 SSW:
* 3 × 1 g Spiramycin/Tag ** 50 mg Pyrimethamin/Tag + 2 × 1,5 g Sulfadiazin/Tag + 2 × 25 mg Folinsäure/Woche alternativ bei fehlender Verfügbarkeit: Cotrimoxazol und Folinsäure oder Pyrimethamin, Azithromyzin und Folinsäure |
|
|
|
Kanada |
SOGC [8] |
2018 |
Clinical Practice Guideline |
|
maternale Infektion in der Schwangerschaft ohne fetale Infektion:
bestätigte oder hochgradig vermutete fetale Infektion:
* 3 × 1 g Spiramycin/Tag, keine Angaben zur Dauer ** keine Angaben zu Dosierung und Dauer |
|
keine Angaben |
|
Österreich |
Arbeitsgruppe Infektiologie der Österreichischen Gesellschaft für Kinderheilkunde [65] |
2013 |
Richtlinie |
|
Therapie der akuten Toxoplasma-gondii-Infektion während der Schwangerschaft:
weitere Therapie je nach AC: positive PCR aus Fruchtwasser oder AC nicht erfolgt:
negative PCR aus Fruchtwasser:
* 3 × 750 mg Spiramycin/Tag ** 25 mg Pyrimethamin/Tag (an Tag 1 50 mg) + 1 × 750 mg Sulfadiazin/Tag (Tag 1 3 × 500 mg) + 3 × 15 mg Folinsäure/Woche |
|
|
|
USA |
Committee on infectious Diseases (American Academy of Pediatrics) Maldonado et al. [34] |
2017 |
Review mit Therapieempfehlungen des PAMF-TSL (Palo Alto Medical Foundation Toxoplasma Serology Laboratory) |
|
Therapie der akuten Toxoplasma-gondii-Infektion mit maternalem Infektionszeitpunkt zwischen 3 Monate präkonzeptionell und 18 + 0 SSW:
falls AC negativ:
falls AC positiv oder sonografisch V. a. fetale Infektion:
Therapie der akuten Toxoplasma-gondii-Infektion mit maternalem Infektionszeitpunkt nach 18 + 0 SSW:
* 3 × 1 g Spiramycin/Tag ** 50 mg Pyrimethamine/Tag (an Tag 1 u. 2 2 × 50 mg/Tag) + 2 × 50 mg/kgKG Sulfadiazin/Tag (max. 4 g/Tag; Tag 1 2 × 37,5 mg/kgKG) + 10 – 12 mg Folinsäure/Tag (bis 1 Woche nach Pyrimethamin-Therapie) |
|
monatliche Ultraschallkontrollen |
|
International |
ISUOG (The International Society of Ultrasound in Obstetrics and Gynecology [36] |
2020 |
Practice Guideline |
|
Therapie der akuten Toxoplasma-gondii-Infektion während der Schwangerschaft:
falls AC positiv:
* 3 × 1 g Spiramycin/Tag ** 50 mg Pyrimethamin/Tag + 3 × 1 g Sulfadiazin/Tag + 50 mg Folinsäure/Woche |
|
|
|
Deutschland |
RKI (Robert Koch-Institut) [1] |
2018 |
Ratgeber |
|
Therapie der akuten Toxoplasma-gondii-Infektion während der Schwangerschaft:
bei auffälligem Ultraschall:
* 3 g (9MIO I. E.) Spiramycin/Tag ** 25 mg Pyrimethamin/Tag (an Tag 1 50 mg) + 50 mg/kgKG Sulfadiazin/Tag (3 g/Tag < 80 kgKG, 4 g/Tag > 80 kgKG) + 10 – 15 mg Folinsäure/Tag |
|
|
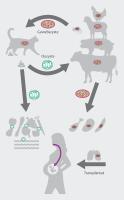

Die Aufnahme von mit Oozysten kontaminierter Nahrung oder Wasser [2] führt bei Zwischenwirten (alle Warmblüter, inkl. Schlachttiere, Vögel und Menschen) primär zur Infektion des Darmepithels und anschließend nach hämatogener Ausbreitung zu lebenslanger Persistenz als Zysten mit replikationsarmen Bradyzoiten in verschiedenen Geweben (vor allem im Gehirn, aber auch in Retina, Skelett- und Herzmuskulatur) [1]. Infizierte Menschen erlangen nach Primärinfektion Immunität, jedoch kann es bei Immunsuppression (z. B. Patient*innen mit AIDS oder Transplantatempfänger) zu einer Reaktivierung kommen.
Die Infektion des Menschen erfolgt durch perorale Aufnahme von sporulierten Oozysten (z. B. nach Gartenarbeit durch ungewaschene Hände oder auf ungewaschenem Gemüse) oder Gewebszysten mit vitalen Bradyzoiten (rohes oder ungenügend behandeltes Fleisch). Ein seltener Übertragungsweg stellt der Empfang von infizierten Transplantaten dar [3].
In Deutschland wird als Hauptinfektionsrisiko der Konsum von rohen Fleischprodukten wie Rohwurst und Mett („Hackepeter“) vermutet. Weitere Risikofaktoren sind ein erhöhter Body-Mass-Index (BMI) und das Halten von Hauskatzen [2].
In Deutschland sind mehr als die Hälfte der Frauen im gebärfähigen Alter seronegativ und können sich in der Schwangerschaft erstmalig mit Toxoplasma gondii infizieren.
Neben den genannten Übertragungswegen kann es bei Erstinfektion in der Schwangerschaft zu einer konnatalen Toxoplasma-Infektion kommen.
Es wird davon ausgegangen, dass ein Drittel der Weltbevölkerung eine Toxoplasma-gondii-Infektion durchgemacht hat [4]. Die Seroprävalenz unter gebärfähigen Frauen in Deutschland nimmt nach einer Auswertung des RKI (Robert Koch-Institut) aus den Jahren 2008 – 2011 mit dem Alter von ca. 20% (18 – 29 Jahre) auf fast 50% (40 – 49 Jahre) zu ([Abb. 2]) [2]. In einem Kollektiv aus schwangeren Frauen in Deutschland lag sie 1992 bei 39% (n = 5670, Alter 15 – 47 Jahre) [5].


Die Inzidenz einer Serokonversion in der Schwangerschaft wird auf 1325/100 000 Schwangerschaften geschätzt (d. h. 1% der Schwangerschaften) [2], wobei nach einer Auswertung von Krankenkassendaten nur in 40/100 000 Schwangerschaften die akute Toxoplasmose-Infektion bekannt ist [6].
4 Maternale Symptome
Eine Toxoplasma-gondii-Infektion verläuft bei immunkompetenten Schwangeren in der Regel asymptomatisch.
In weniger als 10% der Infektionen kommt es bei immunkompetenten Erwachsenen nach einer 1- bis 3-wöchigen Inkubationszeit zu mononukleoseähnlichen Symptomen: Fieber, Kopfschmerz und eine zervikale/okzipitale Lymphadenopathie, die über Wochen persistieren kann. Selten zeigen sich bei Immunkompetenten ein makulopapulöser Ausschlag, eine reaktive Arthritis, eine Hepatosplenomegalie und weitere Organauffälligkeiten [4], [7].
Bei immunsupprimierten Schwangeren kann Toxoplasma gondii zu schwerer Enzephalitis, Myokarditis, Pneumonitis oder Hepatitis führen [8].
5 Konnatale Toxoplasmose
Bei einer Erstinfektion von zuvor seronegativen Müttern oder einer selten vorkommenden Reaktivierung von Toxoplasma gondii im Falle von schwerer Immunsuppression bei seropositiven Frauen in der Schwangerschaft kann es zu einer transplazentaren Infektion des Fetus kommen. Die maternofetale Transmission erfolgt zwischen 1 und 4 Monate nach plazentarer Kolonisation durch Toxoplasma gondii [8]. Die Plazenta stellt dabei sowohl eine Barriere als auch ein Reservoir für Toxoplasmen dar [9].
5.1 Epidemiologie der konnatalen Toxoplasmose
Die maternofetale Übertragungsrate von Toxoplasma gondii steigt mit dem Gestationsalter an, wobei das Risiko für schwere fetale Erkrankungen mit zunehmender Schwangerschaftsdauer abnimmt.
Insgesamt werden pro Jahr in Deutschland ca. 6 – 23 Fälle einer konnatalen Toxoplasmose an das RKI gemeldet [1], wobei eine Auswertung von Krankenkassendaten für den gleichen Bewertungszeitraum auf 43 – 116 diagnostizierte Fälle jährlich kam. Es wird allgemein von einer hohen Dunkelziffer (z. B. durch Aborte und asymptomatische Verläufe) von fetalen Infektionen ausgegangen, und die tatsächliche Anzahl einer konnatalen Toxoplasmose dürfte bei ca. 1300 asymptomatischen und 350 symptomatischen Fällen pro Jahr liegen [2].
Wie bei anderen Infektionskrankheiten auch steigt die maternofetale Übertragungsrate von Toxoplasma gondii mit dem Gestationsalter an ([Abb. 3]), wobei das Risiko für schwere fetale Erkrankungen mit zunehmender Schwangerschaftsdauer abnimmt ([Abb. 4]). Die Daten über maternofetale Transmissionsraten kommen aus Studien, in denen der Großteil der infizierten Mütter nach Diagnosestellung medikamentös behandelt wurde.




Mit dem in Deutschland häufig angewandten medikamentösen Schema wurden Transmissionsraten von 1,3% bei maternaler Infektion im 1. Trimenon, 10,6% im 2. Trimenon und 21,7% im 3. Trimenon angegeben [10].
5.2 Fetale und neonatale Symptome
Die typische Trias einer symptomatischen konnatalen Toxoplasma-gondii-Infektion wurde in den 1950er-Jahren erstmalig von Dr. Albert Sabin [11] beschrieben und besteht aus Retinochoroiditis, zerebralen Verkalkungen und Hydrozephalus.
Daten aus Frankreich (2006 – 2017, [Abb. 5]) zeigen, dass bei pränatalem Screening und Therapie lebendgeborene Kinder mit konnataler Toxoplasma-gondii-Infektion bei Geburt zu 90,7% asymptomatisch und 9,3% symptomatisch sind. Die symptomatischen Kinder zeigen zu ⅔ moderate Symptome (intrakraniale Verkalkungen, periphere Retinochoroiditis) und zu ⅓ schwere Symptome (disseminierte Toxoplasmose, Hydrozephalus oder Retinochoroiditis im Bereich der Makula) [12].


Schwere Formen der konnatalen Toxoplasmose mit Hydrozephalus scheinen nur nach maternaler Infektion im 1. und 2. Trimenon aufzutreten [13], wohingegen eine Retinochoroiditis auch nach Infektion im 3. Trimenon auftreten kann [10], [14].
In Abhängigkeit von Therapiebeginn und -art bestehen in der Literatur große Unterschiede zwischen den Angaben zum Anteil symptomatisch erkrankter Neugeborener.
5.2.1 Retinochoroiditis
Augenläsionen (Toxoplasmen-Retinochoroiditis) können bei konnataler Toxoplasmose auch mehrere Jahre nach der Geburt erstmalig auftreten.
Kinder mit konnataler Toxoplasmose entwickeln in 15,5 – 26% der Fälle eine Retinochoroiditis [15], [16], [17], [18]. Die Daten stammen aus Studien, in denen die Kinder überwiegend prä- und/oder postnatal antiparasitär medikamentös behandelt wurden.
Einschränkungen der Sehkraft im stärker betroffenen Auge treten bei 29% der Kinder mit Toxoplasmen-Retinochoroiditis auf [19]. Schwere beidseitige Einschränkungen der Sehkraft sind selten (9%) [20], [21]. Augenläsionen können auch nach Jahren erstmalig auftreten (39% bei Geburt, 85% vor dem 5. Lebensjahr, 96% vor dem 10. Lebensjahr) [16].
Der Einfluss einer konnatalen Toxoplasmose auf die Lebensqualität wurde in einer Studie mit 102 Patienten (davon 12,7% mit Verminderung der Sehkraft) als gering beschrieben [22], wohingegen Roizen et al. bei 16 Kindern mit Verminderung der Sehkraft auch eine Verminderung von kognitiven Fähigkeiten im Vergleich zu 48 Kindern ohne Verminderung der Sehkraft feststellte [23].
5.2.2 Neurologisches Outcome
Eine symptomatische konnatale Toxoplasmose kann schwere neurologische Folgen wie einen Hydrozephalus und/oder eine psychomotorische Retardierung haben. Diese sind durch prä- und postnatale medikamentöse Therapien selten geworden.
Heinz Eichenwald beschrieb im Jahr 1960 ein unbehandeltes Kollektiv aus Kindern nach Toxplasmosa-gondii-Infektion in der Schwangerschaft, die bei Geburt generalisierte oder neurologische Symptome hatten. Im 4-Jahres-Follow-up zeigten sich in > 85% eine mentale Retardierung, in 81% Krampfanfälle, in 70% motorische Behinderungen, in 60% schwere visuelle Einschränkungen und in 33% Hydrozephalus oder Mikrozephalus. Nur 11% der Kinder zeigten keine Symptome [24].
In aktuelleren Publikationen wird überwiegend das Outcome von intrauterin und/oder postnatal behandelten Kindern beschrieben. Dabei wird z. B. die Prävalenz eines Hydrozephalus nur noch mit 4% der symptomatischen Neugeborenen angegeben [25]. Auch bei Hotop et al. hatten nur 2 von 11 Feten in utero einen Hydrozephalus (alle mit spätem Therapiestart > 8 Wochen), wobei bei Geburt nur noch bei einem Kind ein diskreter Restbefund vorhanden war.
Wallon et al. beschrieben 2004 ein Kollektiv aus 327 Kindern mit nachgewiesener konnataler Toxoplasmose [21]. In 38% der Fälle erfolgte eine intrauterine und in 72% der Fälle eine postnatale Therapie mit Pyrimethamin und Sulfadiazin. Nach einem medianen Follow-up von 6 Jahren hatten 24% retinale Läsionen, 9% zerebrale Kalzifikationen, 2% einen Hydrozephalus und < 1% einen Mikrozephalus. Drei der 6 Kinder mit Hydrozephalus hatten eine moderate psychomotorische Retardierung, die anderen 3 eine normale Entwicklung. Bei 2 der 31 Kinder mit zerebralen Kalzifikationen war es zu einem einmaligen Krampfereignis gekommen. McLone et al. beschrieben 65 Kinder mit Hydrozephalus bei konnataler Toxoplasmose. Das symptomatische Spektrum reichte von normaler kognitiver Funktion bis zu schweren Entwicklungsstörungen. Eine frühzeitige ventrikuloperitoneale Shunteinlage (< 25 Tage nach Diagnose) verbesserte das Outcome. Trotzdem waren ca. 30% der Kinder in dieser Gruppe kognitiv zu eingeschränkt, um an den formalen Intelligenztests teilzunehmen [26].
Es gibt Berichte, dass außerhalb von Europa und den USA vorkommende Subtypen von Toxoplasma gondii zu schwereren klinischen Manifestationen bei Kindern führen können [19], [27], [28].
6 Diagnostik
6.1 Maternale serologische Diagnostik
Alle serologischen Toxoplasmose-Befunde sollen im Mutterpass dokumentiert werden.
Eine Primärinfektion mit Toxoplasma gondii in der Schwangerschaft kann serologisch entweder durch eine Serokonversion bei vorheriger Seronegativität nachgewiesen oder durch Abschätzung des Infektionszeitpunktes mittels Aviditätsanalysen und Serumverlaufskontrollen vermutet werden.
Jeder positive IgM-Antikörper-(Ak-)Nachweis bei einer Schwangeren soll durch ein Speziallabor weiter abgeklärt werden.
Die Diagnose einer maternalen Primärinfektion mit Toxoplasma gondii in der Schwangerschaft kann durch Nachweis von Toxoplasma-gondii-spezifischen Antikörpern bei einer vorher seronegativen Patientin sicher gestellt werden („Serokonversion“) [29].
Liegen keine negativen Vorbefunde in der Schwangerschaft vor, ist bei einem Nachweis von Toxoplasma-spezifischen IgG-Ak vor 18 SSW und gleichzeitiger Seronegativität für Toxoplasma-spezifische IgM-Ak eine Immunität der Schwangeren (i. S. von Schutz für das Kind) durch erfolgte Infektion vor der Schwangerschaft wahrscheinlich[29]. Seltene Ausnahmen sind Toxoplasma-gondii-Infektion mit nur „flüchtiger“ bzw. ohne IgM-Ak-Bildung oder Toxoplasma-gondii-Reaktivierung bei Immunsuppression bzw. -Re-Infektion mit einem virulenten Stamm [30].
In sehr seltenen Einzelfällen wurden Re-Infektionen oder Reaktivierungen bei Schwangeren beschrieben. Dabei schienen einerseits virulentere (atypische) Toxoplasma-Stämme und andererseits der Immunstatus eine wichtige Rolle zu spielen [31], [32].
Bei einem Nachweis von IgG-Ak erstmalig nach 18 SSW oder dem Nachweis von IgM-Ak soll eine weitere Abklärung mittels serologischer Zusatztests (z. B. IgG-Avidität, Immunoblot, IgA-Tests, Analyse von älteren Rückstellproben) durch ein Labor mit entsprechender Expertise erfolgen, um eine akute Infektion in der Schwangerschaft mit fetaler Gefährdung von einer Infektion vor der Schwangerschaft ohne fetale Gefährdung zu unterscheiden (siehe auch RKI-Ratgeber Toxoplasmose [1]).
Dies ist insbesondere von Bedeutung, da IgM im Einzelfall jahrelang persistieren können und daher ein positiver IgM-Befund (insbesondere niedrige IgM-Titer) nicht immer mit einer akuten Toxoplasma-Infektion gleichzusetzen ist. In einer amerikanischen Studie wurde bei positivem IgM-Befund in einem Nichtreferenzlabor nur in 40% der Fälle in einem Referenzlabor eine akute Infektion bestätigt [33].
6.2 Amniozentese
Unter Risiko-Nutzen-Abwägung kann eine Amniozentese durchgeführt werden, wenn das Ergebnis von Entscheidungsrelevanz für die Einleitung einer Therapie ist.
Mittels Amniozentese und Polymerase-Kettenreaktion (PCR) von Toxoplasma-DNA aus Fruchtwasser kann eine fetale Infektion diagnostiziert werden.
Die meisten Daten zur Sensitivität und Spezifität sowie zum negativen prädiktiven Wert liegen für Amniozentesen vor, die mindestens 4 Wochen nach Primärinfektion der Mutter (d. h. 2 Wochen nach der maternalen Serokonversion) und ab 18 + 0 SSW durchgeführt wurden. Diese Zeiträume werden in französischen, kanadischen und US-amerikanischen Empfehlungen sowie vom RKI als Voraussetzung für eine Amniozentese genannt [1], [8], [34], [35]. Eine Begründung ist, dass ab diesem Zeitraum die fetale Urinproduktion ausreichend ist, um eine fetale Toxoplasma-Infektion im Fruchtwasser nachweisen zu können [36].
Die allgemeine Sensitivität der Toxoplasma-PCR aus einer Amniozentese in der Schwangerschaft liegt je nach Studie bei 69 – 92%. Daher schließt eine negative PCR eine fetale Infektion nicht generell aus. Auch wenn im 1. Trimenon die geringste Sensitivität (56,7% [37]) erreicht wird, nimmt der negative prädiktive Wert mit ansteigender Wahrscheinlichkeit für eine fetale Infektion in einigen Studien mit dem Gestationsalter ab (1. Trimenon: 98 – 99%; 2. Trimenon: 92 – 99%; 3. Trimenon: 56 – 100%) [38], [39], [40], [41].
Die Spezifität der Toxoplasma-gondii-PCR aus Fruchtwasser liegt bei 98 – 100% [38], [39], [40], [41]. Daher beweist ein positiver PCR-Befund in der Regel die fetale Infektion.
Eine vor der Amniozentese begonnene Therapie gegen Toxoplasmose hatte in der Auswertung des österreichischen pränatalen Screening-Programms keinen Einfluss auf die Sensitivität und Spezifität der Amniozentese [42].
In den meisten internationalen Empfehlungen wird grundsätzlich zu einer Amniozentese bei maternaler Toxoplasma-Infektion in der Schwangerschaft geraten, um im Falle einer fetalen Infektion eine Anpassung des medikamentösen Therapieschemas vorzunehmen ([Tab. 1]) und fetale Schädigungen abzuwenden oder zu reduzieren. Prospektiv randomisierte Studien hierzu fehlen bislang. Einschränkungen werden teilweise für eine Infektion nach 24 SSW bzw. im 3. Trimenon genannt, hier soll das Risiko für Komplikationen einer Amniozentese mitberücksichtigt werden [8], [34]. Das RKI verweist allgemein darauf, auch das Risiko einer Amniozentese zu berücksichtigen (Abortrisiko in aktuellen Metaanalysen ca. 0,1 – 0,3% [43]). Es empfiehlt daher, unabhängig von der Gestationswoche die Indikation zur Amniozentese streng zu stellen und gibt an, dass sie „eventuell erwogen werden kann, wenn das Ergebnis von Entscheidungsrelevanz für die Einleitung einer Therapie ist“. Entsprechend dieser in Deutschland zurückhaltenden Empfehlung zur Amniozentese wurde im Kollektiv von Hotop et al. [10] bei nur 12,1% der maternalen Toxoplasma-Infektionen in der Schwangerschaft eine Amniozentese durchgeführt.
6.3 Fetaler Ultraschall
Bei Nachweis einer maternalen Toxoplasma-gondii-Infektion sollten 4-wöchentliche Ultraschallkontrollen (entsprechende Qualifikation des Untersuchers, z. B. DEGUM-Stufe II, wird vorausgesetzt) zum Ausschluss von Anzeichen einer fetalen Infektion erfolgen.
Wird eine maternofetale Transmission nachgewiesen, sollten die Intervalle auf 2-wöchentlich angepasst werden.
Bei unauffälligen oder unklaren Ultraschallbefunden kann ergänzend eine Magnetresonanztomografie durchgeführt werden.
Die bislang größte Kohorte von Ultraschallauffälligkeiten bei konnatal mit Toxoplasma gondii infizierten Feten beschreibt in 45 von 88 Fällen isolierte zerebrale Anomalien und in 35 von 88 Fällen die Kombination aus zerebralen und extrazerebralen Anomalien. Isolierte extrazerebrale Auffälligkeiten werden in 8 von 88 Fällen genannt [13].
Die häufigsten intrakranialen Läsionen sind hyperechogene Foci, progrediente Ventrikulomegalie und periventrikuläre Abszesse. Diese Ultraschallbefunde traten fast ausschließlich nach Infektion im 1. und 2. Trimenon auf. Hyperechogene Foci präsentieren sich postnatal als Kalzifikationen, die unter Therapie in 75% der Fälle nach 1 Jahr kleiner oder nicht mehr darstellbar sind [44]. Ventrikulomegalie wird als wichtiger prognostischer Faktor für ein schlechtes neurologisches Outcome beschrieben [45].
Extrazerebrale Veränderungen sind insbesondere Flüssigkeitsansammlungen wie Aszites, außerdem Hepato- und Splenomegalie.
Nach Infektion im 3. Trimenon wurde in der oben genannten Kohorte als sonografische Auffälligkeit nur noch in einigen Fällen eine fetale Wachstumsrestriktion diagnostiziert [13].
Eine fetale Retinochoroiditis kann im Ultraschall nicht erfasst werden.
Zeigen sich bei infizierten Feten sonografisch keine Auffälligkeiten, ist in der Mehrzahl der Fälle von einem günstigen Outcome auszugehen. In einer Studie von Berrebi et al. zeigte nur 1 von 36 Kindern ohne Anomalien im Ultraschall nach Erstinfektion im 1. Trimenon im Alter von 1 Jahr eine schwere Form von konnataler Toxoplasmose. Sieben Kinder entwickelten eine Retinochoroiditis ohne relevanten Visusverlust und mit unauffälliger neurologischer Entwicklung [46].
Bei unauffälligen oder unklaren Ultraschallbefunden wird in einigen internationalen Empfehlungen auf die Möglichkeit einer ergänzenden fetalen Magnetresonanztomografie hingewiesen [36], [47]. Im Rahmen von fetalen Zytomegalievirus-Infektionen konnte ein Zusatznutzen der MRT-Untersuchung als Ergänzung zur Ultraschalldiagnostik bei der Detektion von fetalen ZNS-Anomalien gezeigt werden [48]. Für Toxoplasma-Infektionen liegt bislang keine spezifische Evidenz vor.
7 Transmissionsprophylaxe und Therapie
Zur medikamentösen Behandlung der Toxoplasmose in der Schwangerschaft stehen 2 Optionen zur Verfügung.
Zur Transmissionsprophylaxe wird bei fehlenden Hinweisen auf eine fetale Infektion Spiramycin oder nach 14 + 0 bis 15 + 6 SSW die Kombination aus Pyrimethamin, Sulfadiazin und Folinsäure verwendet. Im 1. Trimenon sollen Pyrimethamin und Sulfadiazin aufgrund der Teratogenität nicht verwendet werden.
Die einzige prospektiv randomisierte Studie zur medikamentösen Transmissionsprophylaxe ab 14 + 0 SSW mit Spiramycin vs. Pyrimethamin/Sulfadiazin zeigte einen Trend zur geringeren Transmissionsrate unter Pyrimethamin/Sulfadiazin (ohne statistische Signifikanz, [Abb. 6]). Zerebrale Auffälligkeiten traten zudem nur in der Spiramycingruppe auf [49], was durch die fehlende Liquorgängigkeit von Spiramycin erklärt werden kann [50]. Ein Placeboarm fehlte in dieser Studie.


In einer retrospektiven Auswertung des österreichischen Toxoplasmoseregisters wurde eine 6-fache Reduktion der maternofetalen Transmission bei Behandlungsbeginn nach österreichischem Therapieschema ([Tab. 1]) innerhalb von 4 Wochen nach maternaler Infektion beschrieben ([Abb. 7]) [7].


Gibt es bereits Hinweise auf eine fetale Infektion, wird im 2. und 3. Trimenon die plazentagängigere und liquorgängige Pyrimethamin-/Sulfadiazin-Kombination zur transplazentaren Therapie des Fetus verwendet.
Die Wirkung der medikamentösen Transmissionsprophylaxe und Therapie beschränkt sich auf den Folsäure- und Proteinstoffwechsel replikativer Tachyzoiten, während sie gegen bradyzoitenhaltige Zysten kaum wirksam sind [1].
Als alternative Medikamente für die Behandlung einer Toxoplasmose wurden Clindamycin und Cotrimoxazol beschrieben.
Mehrere retrospektive Studien konnten durch verschiedene Therapieschemata eine Reduktion von klinischen Manifestationen einer fetalen Toxoplasma-Infektion zeigen, insbesondere bei frühem Therapiestart (siehe auch [Abb. 4]) [10], [14], [51], [52]. Prospektiv randomisierte, placebokontrollierte Studien hierzu existieren aus ethischen Gründen nicht.
In Zusammenschau der oben genannten mit zahlreichen weiteren Studien niedriger Evidenz, insbesondere durch methodische Schwächen, sieht der IGeL-Monitor jedoch insgesamt nur indirekte schwache Hinweise auf einen Nutzen einer medikamentösen Toxoxplasmose-Behandlung in der Schwangerschaft in Bezug auf die Transmissionsrate und die Rate klinischer Manifestationen infizierter Kinder [53].
7.1 Spiramycin
Spiramycin ist nicht teratogen und kann im 1. Trimenon angewendet werden.
Spiramycin ist ein Makrolidantibiotikum, welches durch Inhibition der Proteinsynthese parasitostatisch wirkt. Es akkumuliert in der Plazenta, wobei der transplazentare Transfer gering ist. Seltene Kontraindikationen sind unter anderem Glukose-6-Phosphat-Dehydrogenase-Mangel der Erythrozyten (Gefahr der akuten Hämolyse) und Long-QT-Syndrom.
7.2 Pyrimethamin, Sulfadiazin und Folinsäure
Pyrimethamin und Sulfadiazin sind teratogen und sollen nicht vor dem 2. Trimenon angewendet werden.
Unter Therapie sowie bis 2 Wochen nach Therapie mit Pyrimethamin sollten wöchentliche Blutbildkontrollen (Differenzialblutbild) zum Ausschluss einer Knochenmarksdepression erfolgen (siehe Fachinformation).
Unter Therapie mit Pyrimethamin und Sulfadiazin sollte auf eine ausreichende Flüssigkeitszufuhr geachtet werden (> 2 Liter/Tag bzw. mindestens 1,2 Liter Urinproduktion/Tag), um das Risiko für eine Kristallurie zu reduzieren.
Unter Therapie mit Pyrimethamin und Sulfadiazin soll Folsäure abgesetzt werden und zur Prävention hämatologischer Toxizität durch Folinsäure (Kalziumfolinat) ersetzt werden.
Pyrimethamin und Sulfadiazin wirken synergistisch und hemmen die Folsäuresynthese der Erreger durch Inhibition der Dihydropteroinsäuresynthetase. Aufgrund der Teratogenität sollte diese Therapie nicht im 1. Trimenon erfolgen.
Um das Risiko einer Knochenmarksdepression (Anämie, Leukopenie, Thrombopenie) unter einer Therapie mit Pyrimethamin zu reduzieren, soll während der Therapie die Einnahme von Folinsäure (Kalziumfolinat) erfolgen. Die in der Schwangerschaft übliche Nahrungsergänzung mit Folsäure sollte abgesetzt werden, um die therapeutische Selektivität von Pyrimthemain und Sulfadiazin gegen den Parasiten zu gewährleisten.
Sulfadiazin sollte nicht alleine verwendet werden. Zu den möglichen Nebenwirkungen von Sulfadiazin gehören Hypersensitivitätsreaktionen unterschiedlichen Schweregrades (meist Spätreaktionen), sehr selten auch ein Stevens-Johnson-Syndrom und eine toxisch epidermale Nekrolyse. Sulfadiazin darf bei angeborenem Glukose-6-Phosphat-Dehydrogenase-Mangel der Erythrozyten nicht angewandt werden. Die Gabe von Sulfonamiden in der Schwangerschaft kann insbesondere bei Frühgeborenen das Risiko einer Hyperbilirubinämie erhöhen.
7.3 Clindamycin
In prospektiv randomisierten Studien zur Behandlung einer Toxoplasmose-Enzephalitis bei nicht schwangeren HIV-Patienten wurde Clindamycin als Alternative zu Sulfadiazin in Kombination mit Pyrimethamin und Folinsäure untersucht. Die Daten deuten darauf hin, dass die Clindamycin-/Pyrimethamin-/Folinsäure-Kombination besser verträglich ist als die Sulfadiazin-/Pyrimethamin-/Folinsäure-Kombination bei gleicher Effektivität in Bezug auf den akuten Behandlungseffekt der Toxoplasmose-Enzephalitis, jedoch häufiger zu Rückfällen während der Erhaltungstherapie führt [54]. Für die Behandlung bzw. Transmissionsprophylaxe in der Schwangerschaft liegen lediglich Daten aus einem Mausmodell vor, bei dem die Monotherapie mit Clindamycin eine transplazentare Transmission verhinderte [55].
7.4 Cotrimoxazol
In einer aktuellen retrospektiven Studie wurde die Effektivität der Kombinationsbehandlung Spiramycin/Cotrimoxazol (n = 97) im Vergleich zu Pyrimethamin/Sulfadiazin (n = 8) oder Spiramycin als Monotherapie (n = 64) analysiert [56]. Es zeigte sich kein signifikanter Unterschied zwischen den beiden Kombinationsschemata, die Spiramycin-Monotherapie führte jedoch zu signifikant höheren maternofetalen Transmissionsraten. Die geringe Fallzahl und das retrospektive Design der Studie erscheinen nicht ausreichend, um eine allgemeine Empfehlung zur Behandlung mit Cotrimoxazol in der Schwangerschaft auszusprechen.
7.5 Therapieschemata
7.5.1 Transmissionsprophylaxe
Zur Transmissionsprophylaxe bei akuter maternaler Toxoplasma-gondii-Infektion in der Schwangerschaft ohne Hinweis auf eine fetale Infektion sollte baldmöglichst folgendes Schema verwendet werden:
Bis 14 + 6 SSW:
-
Spiramycin (3,0 g = 9 MIU/Tag)
Ab 15 + 0 SSW (für mindestens 4 Wochen): Kombination aus
-
Pyrimethamin (50 mg am 1. Tag, 25 mg ab 2. Tag) +
-
Sulfadiazin (50 mg/kgKG/Tag; 3 g/Tag bei < 80 kgKG; 4 g/Tag bei ≥ 80 kgKG) +
-
Folinsäure (10 – 15 mg/Tag, Folsäure absetzen)
Zur Transmissionsprophylaxe wird im 1. Trimenon Spiramycin in der Dosierung 9 Mio I. E. pro Tag verwendet. Ob und ab wann ein Wechsel auf Pyrimethamin und Sulfadiazin erfolgt, wird international unterschiedlich empfohlen ([Tab. 1]). Die oben genannte prospektiv-randomisierte Studie von Mandelbrot et al. [49] gibt Hinweise darauf, dass Pyrimethamin und Sulfadiazin bei der Transmissionsprophylaxe effektiver als Spiramycin sein könnten. Als Zeitpunkt des Wechsels auf Pyrimethamin und Sulfadiazin empfiehlt das RKI 15 + 0 SSW [1].
Zur Dauer der Transmissionsprophylaxe bei fehlenden Hinweisen auf eine fetale Infektion (Ultraschallauffälligkeiten oder – falls durchgeführt – positive Amniozentese) mit Pyrimethamin und Sulfadiazin gibt es aufgrund fehlender Evidenz durch prospektiv-randomisierte Studien ebenfalls international sehr unterschiedliche Empfehlungen. In Österreich wird (falls auf eine Amniozentese verzichtet wurde) Pyrimethamin und Sulfadiazin alternierend mit Spiramycin bis zum Ende der Schwangerschaft gegeben. In der französischen Studie von Mandelbrot et al. wurde Pyrimethamin und Sulfadiazin bei negativer Amniozentese nach 4 Wochen abgesetzt, falls keine Amniozentese erfolgte, nach frühestens 8 Wochen. In Deutschland empfiehlt das RKI eine Dauer der Prophylaxe mit Pyrimethamin und Sulfadiazin von mindestens 4 Wochen (unabhängig davon, ob eine Amniozentese durchgeführt wurde). In einer großen deutschen retrospektiven Untersuchung von Hotop et al.[10] wurde die Pyrimethamin-Sulfadiazin-Prophylaxe bei maternalem Infektionszeitpunkt nach 15 + 0 SSW auf 6 Wochen verlängert. Eine Amniozentese wurde in diesem Kollektiv nur bei 83 von 685 (12%) der Schwangeren durchgeführt. Die adjustierte Transmissionsrate in dieser Kohorte war im Vergleich zu französischen Studien [17], [18], [49] niedriger (11% vs. 18 – 30%), und vergleichbar zur Transmissionsrate in Österreich (13%) [7].
Der Anteil an symptomatischen Kindern bei Geburt war in der deutschen Kohorte im Vergleich zu der französischen und der österreichischen höher (33% vs. 13 – 20% bzw. 17%), auch wenn ein Vergleich beispielsweise durch unterschiedliche Häufigkeiten der Infektionen pro Trimenon zwischen den Studien nur eingeschränkt möglich ist.
7.5.2 Therapie bei Verdacht auf oder bereits nachgewiesener fetaler Infektion
Bei gesicherter oder hochgradigem Verdacht auf eine fetale Infektion sollte die Therapie mit Pyrimethamin, Sulfadiazin und Folinsäure bis zur Geburt fortgesetzt werden.
Im Falle von Ultraschallauffälligkeiten, die auf eine Toxoplasma-gondii-Infektion des Fetus hindeuten, oder einem Erregernachweis im Fruchtwasser sollte die Therapie mit Pyrimethamin, Sulfadiazin und Folinsäure bis zur Geburt fortgesetzt werden.
7.5.3 Alternative Behandlungsschemata
Bei fehlender Verfügbarkeit oder Unverträglichkeit von Sulfadiazin können folgende alternativen Behandlungsschemata zur Transmissionsprophylaxe und Therapie eingesetzt werden:
Ab 15 + 0 SSW: Kombination aus
-
Spiramycin (3,0 g = 9 MIU/Tag) +
-
Cotrimoxazol (2 × 960 mg/Tag) +
-
Folinsäure (10 – 15 mg/Tag, Folsäure absetzen)
oder
-
Cotrimoxazol (2 × 960 mg/Tag) +
-
Folinsäure (10 – 15 mg/Tag, Folsäure absetzen)
oder
-
Pyrimethamin (50 mg/Tag) +
-
Clindamycin (3 × 600 mg/Tag) +
-
Folinsäure (10 – 15 mg/Tag, Folsäure absetzen)
Der Bezug von Sulfadiazin kann erschwert bzw. verzögert sein. Um Behandlungsverzögerungen zu vermeiden, können folgende alternative Behandlungsschemata eingesetzt werden: die Kombinationen aus Spiramycin, Cotrimoxazol und Folinsäure (adaptiert nach Buonsenso et al. [56]; in der Originalpublikation wird vor 13 + 0 SSW mit Spiramycin begonnen und Cotrimoxazol/Folinsäure ab 13 + 0 SSW bis eine Woche vor Entbindung mit Spiramycin zusammen gegeben) oder Cotrimoxazol/Folinsäure (adaptiert nach französischer Expertenmeinung [47]; in der Publikation wird Cotrimoxazol/Folinsäure ab 14 + 0 SSW zur Transmissionsprophylaxe eingesetzt und bei fetaler Infektion oder später maternaler Infektion ab 33 + 0 SSW bis zur Geburt fortgesetzt, bei maternaler Infektion vor 33 + 0 SSW und negativer Amniozentese durch Spiramycin bis zur Geburt ersetzt) oder Pyrimethamin, Clindamycin und Folinsäure (Expertenmeinung analog zur Behandlung der Toxoplasmose-Enzephalitis bei HIV [57]; ab 15 + 0 SSW für mindestens 4 Wochen).
Über die Effektivität der 3 Therapieschemata in der Schwangerschaft liegen nur wenige bzw. keine ausreichenden Daten vor, sodass diese Kombinationen nicht als Schemata der ersten Wahl, sondern nur bei Fehlen von Sulfadiazin nach Aufklärung über einen individuellen Heilversuch verwendet werden sollte.
7.6 Zeitpunkt des medikamentösen Behandlungsbeginns
Besteht eine Indikation für eine medikamentöse Toxoplasmose-Behandlung in der Schwangerschaft, soll diese umgehend begonnen werden.
Verschiedene Studien zeigen einen Einfluss des Zeitpunktes der medikamentösen Behandlung auf die maternofetalen Transmissionraten und/oder den Anteil an symptomatischen Feten. Dabei konnte ein z. T. signifikanter Vorteil eines Behandlungsbeginns vor 3 [15] (bzw. 4 [10], [52] oder 8 [14]) Wochen nach maternaler Infektion im Vergleich zu nach 4 [52] bzw. 8 [10], [14], [15] Wochen nach maternaler Infektion gezeigt werden.
7.7 Medikamentenspiegel
Es besteht eine hohe Variabilität bei den Medikamentenspiegeln von Sulfadiazin und Pyrimethamin im mütterlichen Blut. Eine serologische Kontrolle ab 2 Wochen nach Therapiebeginn kann sinnvoll sein.
In einer retrospektiven Fallkontrollstudie mit 89 Frauen mit Toxoplasma-Primärinfektion in der Schwangerschaft und 17 nicht schwangeren Frauen mit akuter okulärer Toxoplasmose zeigten sich bei den schwangeren Frauen in 26% der Fälle Sulfadiazin-Spiegel unter 20 mg/l und in 17% der Fälle zusätzlich Pyrimethamin-Spiegel unter 700 µg/l [58]. Aufgrund fehlender Studien bleibt unklar, welche therapeutischen Bereiche bei Schwangeren eingesetzt werden sollten. Es wird davon ausgegangen, das im fetalen Blut ⅓ der maternalen Pyrimethamin-Level erreicht werden können [59]. Bei nicht schwangeren Patienten werden bei der Kombinationsbehandlung mit Sulfadiazin und Pyrimethamin therapeutische Bereiche von 50 – 150 mg/l für Sulfadiazin und 700 – 1300 µg/l für Pyrimethamin angegeben [58].
8 Prävention
Seronegative Schwangere sollen über Hygienemaßnahmen zur Expositionsprophylaxe gegenüber Toxoplasma gondii beraten werden.
Seronegative Schwangere können durch eine Expositionsprophylaxe das Risiko für eine Infektion mit Toxoplasma gondii verringern [60]. Zu den Präventionsmaßnahmen gehören [1], [8]:
-
keine rohen oder nicht ausreichend erhitzten oder gefrosteten Fleischprodukte (z. B. Hackepeter oder kurz gereifte Rohwürste) essen,
-
rohes Gemüse und Früchte vor dem Verzehr gründlich waschen,
-
Waschen der Hände vor dem Essen,
-
Waschen der Hände nach dem Zubereiten von rohem Fleisch, nach Garten-, Feld- oder anderen Erdarbeiten und nach dem Besuch von Sandspielplätzen,
-
bei Halten einer Katze innerhalb der Wohnung in der Umgebung der Schwangeren sollte diese nur mit Dosen und/oder Trockenfutter ernährt werden. Die Kotkästen, insbesondere frei gehaltener Katzen, sollten täglich durch Nichtschwangere mit heißem Wasser gereinigt werden.
Hierüber soll im Rahmen der Schwangerenvorsorge entsprechend den Mutterschafts-Richtlinien beraten werden [61].
9 Screening
Nicht immune Schwangere sollen über die Risiken einer Toxoplasma-gondii-Infektion und die Möglichkeit eines Toxoplasmose-Screenings informiert werden.
Wird von der Schwangeren ein Toxoplasmose-Screening gewünscht, sollten möglichst früh in der Schwangerschaft der Antikörperstatus (Toxoplasma-IgG und -IgM) überprüft und bei seronegativen Schwangeren alle 4 – 8 Wochen bis zum Ende der Schwangerschaft Verlaufskontrollen zum Ausschluss einer Serokonversion erfolgen.
Ein Screening auf Toxoplasmose in der Schwangerschaft ist in verschiedenen europäischen Ländern bereits Standard (Österreich seit 1974, Frankreich seit 1992, Italien seit 1998 und Slowenien seit 1995). Mehrere Studien haben gezeigt, dass die Einführung von systematischen Screening-Programmen zeitgleich zu einer Reduktion an maternofetalen Transmissionen und fetalen Schädigungen führte und kosteneffektiv ist [62]. Die Screening-Intervalle der verschiedenen Länder bei seronegativen Schwangeren sind unterschiedlich, z. B. monatlich in Frankreich und alle 8 Wochen in Österreich. In der Schweiz hat man sich seit 2008 aufgrund der unklaren Evidenz, der geringen Inzidenz einer konnatalen Toxoplasmose sowie möglicher negativer Folgen (z. B. Verunsicherung der Schwangeren bei falsch positiven Befunden, Komplikationen im Rahmen einer Amniozentese) gegen ein Screening auf Toxoplasmose entschieden [63].
In Deutschland sind serologische Screening-Untersuchungen auf Toxoplasma gondii aktuell ebenfalls keine GKV-Leistung und können daher gesetzlich Krankenversicherten nur als IGeL angeboten werden. Liegt der begründete V. a. eine Infektion vor (z. B. relevante Exposition, Symptome, Ultraschallauffälligkeiten), werden die Tests als kurative Leistung abgerechnet.
Schwangere sollten über diese Möglichkeit, jedoch auch über die unklare Evidenz eines Screenings [53] informiert werden. Wird von der Schwangeren ein Toxoplasmose-Screening gewünscht, sollte möglichst früh in der Schwangerschaft der Antikörperstatus (Toxoplasma-IgG und -IgM) überprüft und bei seronegativen Schwangeren alle 4 – 8 Wochen bis zum Ende der Schwangerschaft Verlaufskontrollen zum Ausschluss einer Serokonversion erfolgen. Dadurch wäre ggf. eine zeitnahe Therapie (siehe 6.5) möglich.
10 Entbindung und Stillen
Die Entbindung bei maternofetaler Toxoplasma-gondii-Infektion sollte nach allgemeinen geburtshilflichen Kriterien erfolgen.
Eine Übertragung von Toxoplasma gondii über die Muttermilch ist beim Menschen bislang nicht belegt.
In einer Studie mit 10 schwangeren Frauen und maternaler Toxoplasma-Infektion kam es trotz zeitnaher Entbindung mittels Einleitung der Geburt oder Sectio caesarea (durchschnittlich 3 Wochen nach maternaler Infektion) zu einer fetalen Infektion in 9 von 10 Fällen. Die Autoren kommen zu dem Schluss, dass eine frühzeitige Entbindung auch bei später maternaler Primärinfektion nicht erfolgen sollte, da eine maternofetale Transmission hierdurch nicht sicher verhindert werden kann [64].
Peripartal sollte eine Information über die erfolgte maternofetale Diagnostik und ggf. Therapie an die pädiatrischen Kollegen erfolgen, um die ggf. notwendige Diagnostik und Therapie beim Neugeborenen zu planen.
Stillen ist bei maternaler Toxoplasma-Infektion möglich, da eine Übertragung von Toxoplasma gondii über die Muttermilch beim Menschen bislang nicht belegt ist.
11 Behandlung des Neugeborenen nach der Geburt
Bei infizierten Neugeborenen stellt ebenfalls die Kombination aus Pyrimethamin, Sulfadiazin und Folinsäure das Behandlungsschema der ersten Wahl dar. Die Behandlungsdauer ist abhängig von der Symptomatik der Neugeborenen (in der Regel 3 – 12 Monate) [1].
Conflict of Interest/Interessenkonflikt
The authors declare that they have no conflict of interest.
-
References/Literatur
- 1 Robert Koch-Institut. RKI-Ratgeber Toxoplasmose. Epidemiol Bull 2018; 42: 451-460
- 2 Wilking H, Thamm M, Stark K. et al. Prevalence, incidence estimations, and risk factors of Toxoplasma gondii infection in Germany: a representative, cross-sectional, serological study. Sci Rep 2016; 6: 22551
- 3 Pleyer U, Groß U, Schlüter D. et al. Toxoplasmosis in Germany: Epidemiology, Diagnosis, Risk Factors, and Treatment. Dtsch Arztebl Int 2019; 116: 435-444
- 4 Montoya JG, Liesenfeld O. Toxoplasmosis. Lancet 2004; 363: 1965-1976
- 5 Beringer T. [Is diagnosis of toxoplasmosis within the scope of prenatal care meaningful?]. Geburtshilfe Frauenheilkd 1992; 52: 740-741
- 6 Krings A, Jacob J, Seeber F. et al. Estimates of Toxoplasmosis Incidence Based on Healthcare Claims Data, Germany, 2011–2016. Emerg Infect Dis 2021; 27: 2097-2106
- 7 Prusa A-R, Kasper DC, Pollak A. et al. The Austrian Toxoplasmosis Register, 1992–2008. Clin Infect Dis 2015; 60: e4-e10
- 8 Paquet C, Yudin MH. No. 285-Toxoplasmosis in Pregnancy: Prevention, Screening, and Treatment. J Obstet Gynaecol Can 2018; 40: e687-e693
- 9 Leruez-Ville M, Benoist G, Ville Y. Fetal Infections: Clinical Management. In: Kilby MD, Johnson A, Oepkes D, eds. Fetal Therapy. Cambridge University Press; 2019: 224-247
- 10 Hotop A, Hlobil H, Gross U. Efficacy of rapid treatment initiation following primary Toxoplasma gondii infection during pregnancy. Clin Infect Dis 2012; 54: 1545-1552
- 11 Dubey JP, Murata FHA, Cerqueira-Cézar CK. et al. Congenital toxoplasmosis in humans: an update of worldwide rate of congenital infections. Parasitology 2021; 148: 1406-1416
- 12 Picone O, Fuchs F, Benoist G. et al. Toxoplasmosis screening during pregnancy in France: Opinion of an expert panel for the CNGOF. J Gynecol Obstet Hum Reprod 2020; 49: 101814
- 13 Codaccioni C, Picone O, Lambert V. et al. Ultrasound features of fetal toxoplasmosis: A contemporary multicenter survey in 88 fetuses. Prenat Diagn 2020; 40: 1741-1752
- 14 Kieffer F, Wallon M, Garcia P. et al. Risk factors for retinochoroiditis during the first 2 years of life in infants with treated congenital toxoplasmosis. Pediatr Infect Dis J 2008; 27: 27-32
- 15 SYROCOT (Systematic Review on Congenital Toxoplasmosis) study group. Thiébaut R, Leproust S. et al. Effectiveness of prenatal treatment for congenital toxoplasmosis: a meta-analysis of individual patientsʼ data. Lancet 2007; 369: 115-122
- 16 Berrébi A, Assouline C, Bessières M-H. et al. Long-term outcome of children with congenital toxoplasmosis. Am J Obstet Gynecol 2010; 203: 552.e1-552.e6
- 17 Dunn D, Wallon M, Peyron F. et al. Mother-to-child transmission of toxoplasmosis: risk estimates for clinical counselling. Lancet 1999; 353: 1829-1833
- 18 Wallon M, Peyron F, Cornu C. et al. Congenital toxoplasma infection: monthly prenatal screening decreases transmission rate and improves clinical outcome at age 3 years. Clin Infect Dis 2013; 56: 1223-1231
- 19 Gilbert RE, Freeman K, Lago EG. et al. Ocular sequelae of congenital toxoplasmosis in Brazil compared with Europe. PLoS Negl Trop Dis 2008; 2: e277
- 20 Tan HK, Schmidt D, Stanford M. et al. Risk of visual impairment in children with congenital toxoplasmic retinochoroiditis. Am J Ophthalmol 2007; 144: 648-653
- 21 Wallon M, Kodjikian L, Binquet C. et al. Long-term ocular prognosis in 327 children with congenital toxoplasmosis. Pediatrics 2004; 113: 1567-1572
- 22 Peyron F, Garweg JG, Wallon M. et al. Long-term impact of treated congenital toxoplasmosis on quality of life and visual performance. Pediatr Infect Dis J 2011; 30: 597-600
- 23 Roizen N, Kasza K, Karrison T. et al. Impact of visual impairment on measures of cognitive function for children with congenital toxoplasmosis: implications for compensatory intervention strategies. Pediatrics 2006; 118: e379-e390
- 24 Eichenwald HF. A study of congenital toxoplasmosis, with particular emphasis on clinical manifestations, sequelae and therapy. In: Siim JC. ed. Human toxoplasmosis. Copenhagen: Munksgaard; 1960: 41-49
- 25 Hutson SL, Wheeler KM, McLone D. et al. Patterns of Hydrocephalus Caused by Congenital Toxoplasma gondii Infection Associate With Parasite Genetics. Clin Infect Dis 2015; 61: 1831-1834
- 26 McLone D, Frim D, Penn R. et al. Outcomes of hydrocephalus secondary to congenital toxoplasmosis. J Neurosurg Pediatr 2019;
- 27 Anand R, Jones CW, Ricks JH. et al. Acute primary toxoplasmosis in travelers returning from endemic countries. J Travel Med 2012; 19: 57-60
- 28 Rudzinski M, Khoury M, Couto C. et al. Reactivation of Ocular Toxoplasmosis in Non-Hispanic Persons, Misiones Province, Argentina. Emerg Infect Dis 2016; 22: 912-913
- 29 Montoya JG, Remington JS. Management of Toxoplasma gondii infection during pregnancy. Clin Infect Dis 2008; 47: 554-566
- 30 Fricker-Hidalgo H, Cimon B, Chemla C. et al. Toxoplasma seroconversion with negative or transient immunoglobulin M in pregnant women: myth or reality? A French multicenter retrospective study. J Clin Microbiol 2013; 51: 2103-2111
- 31 Elbez-Rubinstein A, Ajzenberg D, Dardé M-L. et al. Congenital toxoplasmosis and reinfection during pregnancy: case report, strain characterization, experimental model of reinfection, and review. J Infect Dis 2009; 199: 280-285
- 32 Low incidence of congenital toxoplasmosis in children born to women infected with human immunodeficiency virus. European Collaborative Study and Research Network on Congenital Toxoplasmosis. Eur J Obstet Gynecol Reprod Biol 1996; 68: 93-96
- 33 Liesenfeld O, Montoya JG, Tathineni NJ. et al. Confirmatory serologic testing for acute toxoplasmosis and rate of induced abortions among women reported to have positive Toxoplasma immunoglobulin M antibody titers. Am J Obstet Gynecol 2001; 184: 140-145
- 34 Maldonado YA, Read JS. COMMITTEE ON INFECTIOUS DISEASES. Diagnosis, Treatment, and Prevention of Congenital Toxoplasmosis in the United States. Pediatrics 2017; 139: e20163860
- 35 Peyron F, Lʼollivier C, Mandelbrot L. et al. Maternal and Congenital Toxoplasmosis: Diagnosis and Treatment Recommendations of a French Multidisciplinary Working Group. Pathogens 2019; 8: 24
- 36 Khalil A, Sotiriadis A, Chaoui R. et al. ISUOG Practice Guidelines: role of ultrasound in congenital infection. Ultrasound Obstet Gynecol 2020; 56: 128-151
- 37 de Oliveira Azevedo CT, do Brasil PEAA, Guida L. et al. Performance of Polymerase Chain Reaction Analysis of the Amniotic Fluid of Pregnant Women for Diagnosis of Congenital Toxoplasmosis: A Systematic Review and Meta-Analysis. PloS One 2016; 11: e0149938
- 38 Sterkers Y, Pratlong F, Albaba S. et al. Novel Interpretation of Molecular Diagnosis of Congenital Toxoplasmosis According to Gestational Age at the Time of Maternal Infection. J Clin Microbiol 2012; 50: 3944-3951
- 39 Wallon M, Franck J, Thulliez P. et al. Accuracy of real-time polymerase chain reaction for Toxoplasma gondii in amniotic fluid. Obstet Gynecol 2010; 115: 727-733
- 40 Rabilloud M, Wallon M, Peyron F. In utero and at birth diagnosis of congenital toxoplasmosis: use of likelihood ratios for clinical management. Pediatr Infect Dis J 2010; 29: 421-425
- 41 Thalib L, Gras L, Romand S. et al. Prediction of congenital toxoplasmosis by polymerase chain reaction analysis of amniotic fluid. BJOG Int J Obstet Gynaecol 2005; 112: 567-574
- 42 Prusa A-R, Kasper DC, Pollak A. et al. Amniocentesis for the detection of congenital toxoplasmosis: results from the nationwide Austrian prenatal screening program. Clin Microbiol Infect 2015; 21: 191.e1-191.e8
- 43 Salomon LJ, Sotiriadis A, Wulff CB. et al. Risk of miscarriage following amniocentesis or chorionic villus sampling: systematic review of literature and updated meta-analysis. Ultrasound Obstet Gynecol 2019; 54: 442-451
- 44 Patel DV, Holfels EM, Vogel NP. et al. Resolution of intracranial calcifications in infants with treated congenital toxoplasmosis. Radiology 1996; 199: 433-440
- 45 Blondiaux E, Garel C. Fetal cerebral imaging – ultrasound vs. MRI: an update. Acta Radiol 2013; 54: 1046-1054
- 46 Berrebi A, Bardou M, Bessieres M-H. et al. Outcome for children infected with congenital toxoplasmosis in the first trimester and with normal ultrasound findings: a study of 36 cases. Eur J Obstet Gynecol Reprod Biol 2007; 135: 53-57
- 47 Mandelbrot L, Kieffer F, Wallon M. et al. Toxoplasmose pendant la grossesse: proposition actuelle de prise en charge pratique. Gynecol Obstet Fertil Senol 2021; 49: 782-791
- 48 Di Mascio D, Rizzo G, Khalil A. et al. Role of fetal magnetic resonance imaging in fetuses with congenital cytomegalovirus infection: multicenter study. Ultrasound Obstet Gynecol 2023; 61: 67-73
- 49 Mandelbrot L, Kieffer F, Sitta R. et al. Prenatal therapy with pyrimethamine + sulfadiazine vs. spiramycin to reduce placental transmission of toxoplasmosis: a multicenter, randomized trial. Am J Obstet Gynecol 2018; 219: 386.e1-386.e9
- 50 Schoondermark-van de Ven EM, Melchers WJ, Galama JM. et al. Prenatal diagnosis and treatment of congenital Toxoplasma gondii infections: an experimental study in rhesus monkeys. Eur J Obstet Gynecol Reprod Biol 1997; 74: 183-188
- 51 Cortina-Borja M, Tan HK, Wallon M. et al. Prenatal Treatment for Serious Neurological Sequelae of Congenital Toxoplasmosis: An Observational Prospective Cohort Study. PLoS Med 2010; 7: 11
- 52 Gras L, Wallon M, Pollak A. et al. European Multicenter Study on Congenital Toxoplasmosis. Association between prenatal treatment and clinical manifestations of congenital toxoplasmosis in infancy: a cohort study in 13 European centres. Acta Paediatr 2005; 94: 1721-1731
- 53 Schuster S, Janatzek S, Chittka L. IGeLMonitor- Evidenz ausführlich – Toxoplasmose-Test in der Schwangerschaft. Accessed September 10, 2022 at: https://www.igel-monitor.de/fileadmin/user_upload/Toxoplasmosetest_Schwangerschaft_Evidenz_ausfuehrlich.pdf
- 54 Katlama C, De Wit S, OʼDoherty E. et al. Pyrimethamine-clindamycin vs. pyrimethamine-sulfadiazine as acute and long-term therapy for toxoplasmic encephalitis in patients with AIDS. Clin Infect Dis 1996; 22: 268-275
- 55 Araujo FG, Remington JS. Effect of Clindamycin on Acute and Chronic Toxoplasmosis in Mice. Antimicrob Agents Chemother 1974; 5: 647-651
- 56 Buonsenso D, Pata D, Turriziani Colonna A. et al. Spyramicine and Trimethoprim-Sulfamethoxazole Combination to Prevent Mother-To-Fetus Transmission of Toxoplasma gondii Infection in Pregnant Women: A 28-Years Single-center Experience. Pediatr Infect Dis J 2022; 41: e223-e227
- 57 EACSociety. EACS Guidelines. Accessed September 17, 2022 at: https://www.eacsociety.org/guidelines/eacs-guidelines/
- 58 Reiter-Owona I, Hlobil H, Enders M. et al. Sulfadiazine plasma concentrations in women with pregnancy-acquired compared to ocular toxoplasmosis under pyrimethamine and sulfadiazine therapy: a case-control study. Eur J Med Res 2020; 25: 59
- 59 Peytavin G, Leng JJ, Forestier F. et al. Placental transfer of pyrimethamine studied in an ex vivo placental perfusion model. Biol Neonate 2000; 78: 83-85
- 60 Wehbe K, Pencole L, Lhuaire M. et al. Hygiene measures as primary prevention of toxoplasmosis during pregnancy: A systematic review. J Gynecol Obstet Hum Reprod 2022; 51: 102300
- 61 Gemeinsamer Bundesausschuss. Mutterschafts-Richtlinien. 2021. Accessed April 18, 2023 at: https://www.g-ba.de/downloads/62-492-2676/Mu-RL_2021-09-16_iK-2022-01-01.pdf
- 62 Prusa A-R, Kasper DC, Sawers L. et al. Congenital toxoplasmosis in Austria: Prenatal screening for prevention is cost-saving. PLoS Negl Trop Dis 2017; 11: e0005648
- 63 SGGG. Expertenbrief 31 – Verzicht auf das Toxoplasmose-Screening in der Schwangerschaft – kurze zusammenfassende Begründung. 2010. Accessed September 17, 2022 at: https://www.sggg.ch/fileadmin/user_upload/PDF/31_Toxoplasmose-Screening_2010.pdf
- 64 Wallon M, Kieffer F, Huissoud C. et al. Cesarean delivery or induction of labor does not prevent vertical transmission of toxoplasmosis in late pregnancy. Int J Gynaecol Obstet 2015; 129: 176-177
- 65 Arbeitsgruppe Infektiologie der Österreichischen Gesellschaft für Kinderheilkunde. Österreichische Richtlinie für das Toxoplasmose-Screening in der Schwangerschaft und frühen Kindheit. 2013. Accessed January 21, 2021 at: https://www.oeghmp.at/media/richtlinie_toxoplasmose-screening.pdf
- 66 Wichtige humane Parasitosen: Toxoplasmose. Z Gastroenterol 2020; 58: 742-746
Correspondence/Korrespondenzadresse
Publikationsverlauf
Eingereicht: 14. Juni 2023
Angenommen nach Revision: 18. Juli 2023
Artikel online veröffentlicht:
18. September 2023
© 2023. The Author(s). This is an open access article published by Thieme under the terms of the Creative Commons Attribution-NonDerivative-NonCommercial License, permitting copying and reproduction so long as the original work is given appropriate credit. Contents may not be used for commecial purposes, or adapted, remixed, transformed or built upon. (https://creativecommons.org/licenses/by-nc-nd/4.0/)
Georg Thieme Verlag KG
Rüdigerstraße 14, 70469 Stuttgart, Germany
-
References/Literatur
- 1 Robert Koch-Institut. RKI-Ratgeber Toxoplasmose. Epidemiol Bull 2018; 42: 451-460
- 2 Wilking H, Thamm M, Stark K. et al. Prevalence, incidence estimations, and risk factors of Toxoplasma gondii infection in Germany: a representative, cross-sectional, serological study. Sci Rep 2016; 6: 22551
- 3 Pleyer U, Groß U, Schlüter D. et al. Toxoplasmosis in Germany: Epidemiology, Diagnosis, Risk Factors, and Treatment. Dtsch Arztebl Int 2019; 116: 435-444
- 4 Montoya JG, Liesenfeld O. Toxoplasmosis. Lancet 2004; 363: 1965-1976
- 5 Beringer T. [Is diagnosis of toxoplasmosis within the scope of prenatal care meaningful?]. Geburtshilfe Frauenheilkd 1992; 52: 740-741
- 6 Krings A, Jacob J, Seeber F. et al. Estimates of Toxoplasmosis Incidence Based on Healthcare Claims Data, Germany, 2011–2016. Emerg Infect Dis 2021; 27: 2097-2106
- 7 Prusa A-R, Kasper DC, Pollak A. et al. The Austrian Toxoplasmosis Register, 1992–2008. Clin Infect Dis 2015; 60: e4-e10
- 8 Paquet C, Yudin MH. No. 285-Toxoplasmosis in Pregnancy: Prevention, Screening, and Treatment. J Obstet Gynaecol Can 2018; 40: e687-e693
- 9 Leruez-Ville M, Benoist G, Ville Y. Fetal Infections: Clinical Management. In: Kilby MD, Johnson A, Oepkes D, eds. Fetal Therapy. Cambridge University Press; 2019: 224-247
- 10 Hotop A, Hlobil H, Gross U. Efficacy of rapid treatment initiation following primary Toxoplasma gondii infection during pregnancy. Clin Infect Dis 2012; 54: 1545-1552
- 11 Dubey JP, Murata FHA, Cerqueira-Cézar CK. et al. Congenital toxoplasmosis in humans: an update of worldwide rate of congenital infections. Parasitology 2021; 148: 1406-1416
- 12 Picone O, Fuchs F, Benoist G. et al. Toxoplasmosis screening during pregnancy in France: Opinion of an expert panel for the CNGOF. J Gynecol Obstet Hum Reprod 2020; 49: 101814
- 13 Codaccioni C, Picone O, Lambert V. et al. Ultrasound features of fetal toxoplasmosis: A contemporary multicenter survey in 88 fetuses. Prenat Diagn 2020; 40: 1741-1752
- 14 Kieffer F, Wallon M, Garcia P. et al. Risk factors for retinochoroiditis during the first 2 years of life in infants with treated congenital toxoplasmosis. Pediatr Infect Dis J 2008; 27: 27-32
- 15 SYROCOT (Systematic Review on Congenital Toxoplasmosis) study group. Thiébaut R, Leproust S. et al. Effectiveness of prenatal treatment for congenital toxoplasmosis: a meta-analysis of individual patientsʼ data. Lancet 2007; 369: 115-122
- 16 Berrébi A, Assouline C, Bessières M-H. et al. Long-term outcome of children with congenital toxoplasmosis. Am J Obstet Gynecol 2010; 203: 552.e1-552.e6
- 17 Dunn D, Wallon M, Peyron F. et al. Mother-to-child transmission of toxoplasmosis: risk estimates for clinical counselling. Lancet 1999; 353: 1829-1833
- 18 Wallon M, Peyron F, Cornu C. et al. Congenital toxoplasma infection: monthly prenatal screening decreases transmission rate and improves clinical outcome at age 3 years. Clin Infect Dis 2013; 56: 1223-1231
- 19 Gilbert RE, Freeman K, Lago EG. et al. Ocular sequelae of congenital toxoplasmosis in Brazil compared with Europe. PLoS Negl Trop Dis 2008; 2: e277
- 20 Tan HK, Schmidt D, Stanford M. et al. Risk of visual impairment in children with congenital toxoplasmic retinochoroiditis. Am J Ophthalmol 2007; 144: 648-653
- 21 Wallon M, Kodjikian L, Binquet C. et al. Long-term ocular prognosis in 327 children with congenital toxoplasmosis. Pediatrics 2004; 113: 1567-1572
- 22 Peyron F, Garweg JG, Wallon M. et al. Long-term impact of treated congenital toxoplasmosis on quality of life and visual performance. Pediatr Infect Dis J 2011; 30: 597-600
- 23 Roizen N, Kasza K, Karrison T. et al. Impact of visual impairment on measures of cognitive function for children with congenital toxoplasmosis: implications for compensatory intervention strategies. Pediatrics 2006; 118: e379-e390
- 24 Eichenwald HF. A study of congenital toxoplasmosis, with particular emphasis on clinical manifestations, sequelae and therapy. In: Siim JC. ed. Human toxoplasmosis. Copenhagen: Munksgaard; 1960: 41-49
- 25 Hutson SL, Wheeler KM, McLone D. et al. Patterns of Hydrocephalus Caused by Congenital Toxoplasma gondii Infection Associate With Parasite Genetics. Clin Infect Dis 2015; 61: 1831-1834
- 26 McLone D, Frim D, Penn R. et al. Outcomes of hydrocephalus secondary to congenital toxoplasmosis. J Neurosurg Pediatr 2019;
- 27 Anand R, Jones CW, Ricks JH. et al. Acute primary toxoplasmosis in travelers returning from endemic countries. J Travel Med 2012; 19: 57-60
- 28 Rudzinski M, Khoury M, Couto C. et al. Reactivation of Ocular Toxoplasmosis in Non-Hispanic Persons, Misiones Province, Argentina. Emerg Infect Dis 2016; 22: 912-913
- 29 Montoya JG, Remington JS. Management of Toxoplasma gondii infection during pregnancy. Clin Infect Dis 2008; 47: 554-566
- 30 Fricker-Hidalgo H, Cimon B, Chemla C. et al. Toxoplasma seroconversion with negative or transient immunoglobulin M in pregnant women: myth or reality? A French multicenter retrospective study. J Clin Microbiol 2013; 51: 2103-2111
- 31 Elbez-Rubinstein A, Ajzenberg D, Dardé M-L. et al. Congenital toxoplasmosis and reinfection during pregnancy: case report, strain characterization, experimental model of reinfection, and review. J Infect Dis 2009; 199: 280-285
- 32 Low incidence of congenital toxoplasmosis in children born to women infected with human immunodeficiency virus. European Collaborative Study and Research Network on Congenital Toxoplasmosis. Eur J Obstet Gynecol Reprod Biol 1996; 68: 93-96
- 33 Liesenfeld O, Montoya JG, Tathineni NJ. et al. Confirmatory serologic testing for acute toxoplasmosis and rate of induced abortions among women reported to have positive Toxoplasma immunoglobulin M antibody titers. Am J Obstet Gynecol 2001; 184: 140-145
- 34 Maldonado YA, Read JS. COMMITTEE ON INFECTIOUS DISEASES. Diagnosis, Treatment, and Prevention of Congenital Toxoplasmosis in the United States. Pediatrics 2017; 139: e20163860
- 35 Peyron F, Lʼollivier C, Mandelbrot L. et al. Maternal and Congenital Toxoplasmosis: Diagnosis and Treatment Recommendations of a French Multidisciplinary Working Group. Pathogens 2019; 8: 24
- 36 Khalil A, Sotiriadis A, Chaoui R. et al. ISUOG Practice Guidelines: role of ultrasound in congenital infection. Ultrasound Obstet Gynecol 2020; 56: 128-151
- 37 de Oliveira Azevedo CT, do Brasil PEAA, Guida L. et al. Performance of Polymerase Chain Reaction Analysis of the Amniotic Fluid of Pregnant Women for Diagnosis of Congenital Toxoplasmosis: A Systematic Review and Meta-Analysis. PloS One 2016; 11: e0149938
- 38 Sterkers Y, Pratlong F, Albaba S. et al. Novel Interpretation of Molecular Diagnosis of Congenital Toxoplasmosis According to Gestational Age at the Time of Maternal Infection. J Clin Microbiol 2012; 50: 3944-3951
- 39 Wallon M, Franck J, Thulliez P. et al. Accuracy of real-time polymerase chain reaction for Toxoplasma gondii in amniotic fluid. Obstet Gynecol 2010; 115: 727-733
- 40 Rabilloud M, Wallon M, Peyron F. In utero and at birth diagnosis of congenital toxoplasmosis: use of likelihood ratios for clinical management. Pediatr Infect Dis J 2010; 29: 421-425
- 41 Thalib L, Gras L, Romand S. et al. Prediction of congenital toxoplasmosis by polymerase chain reaction analysis of amniotic fluid. BJOG Int J Obstet Gynaecol 2005; 112: 567-574
- 42 Prusa A-R, Kasper DC, Pollak A. et al. Amniocentesis for the detection of congenital toxoplasmosis: results from the nationwide Austrian prenatal screening program. Clin Microbiol Infect 2015; 21: 191.e1-191.e8
- 43 Salomon LJ, Sotiriadis A, Wulff CB. et al. Risk of miscarriage following amniocentesis or chorionic villus sampling: systematic review of literature and updated meta-analysis. Ultrasound Obstet Gynecol 2019; 54: 442-451
- 44 Patel DV, Holfels EM, Vogel NP. et al. Resolution of intracranial calcifications in infants with treated congenital toxoplasmosis. Radiology 1996; 199: 433-440
- 45 Blondiaux E, Garel C. Fetal cerebral imaging – ultrasound vs. MRI: an update. Acta Radiol 2013; 54: 1046-1054
- 46 Berrebi A, Bardou M, Bessieres M-H. et al. Outcome for children infected with congenital toxoplasmosis in the first trimester and with normal ultrasound findings: a study of 36 cases. Eur J Obstet Gynecol Reprod Biol 2007; 135: 53-57
- 47 Mandelbrot L, Kieffer F, Wallon M. et al. Toxoplasmose pendant la grossesse: proposition actuelle de prise en charge pratique. Gynecol Obstet Fertil Senol 2021; 49: 782-791
- 48 Di Mascio D, Rizzo G, Khalil A. et al. Role of fetal magnetic resonance imaging in fetuses with congenital cytomegalovirus infection: multicenter study. Ultrasound Obstet Gynecol 2023; 61: 67-73
- 49 Mandelbrot L, Kieffer F, Sitta R. et al. Prenatal therapy with pyrimethamine + sulfadiazine vs. spiramycin to reduce placental transmission of toxoplasmosis: a multicenter, randomized trial. Am J Obstet Gynecol 2018; 219: 386.e1-386.e9
- 50 Schoondermark-van de Ven EM, Melchers WJ, Galama JM. et al. Prenatal diagnosis and treatment of congenital Toxoplasma gondii infections: an experimental study in rhesus monkeys. Eur J Obstet Gynecol Reprod Biol 1997; 74: 183-188
- 51 Cortina-Borja M, Tan HK, Wallon M. et al. Prenatal Treatment for Serious Neurological Sequelae of Congenital Toxoplasmosis: An Observational Prospective Cohort Study. PLoS Med 2010; 7: 11
- 52 Gras L, Wallon M, Pollak A. et al. European Multicenter Study on Congenital Toxoplasmosis. Association between prenatal treatment and clinical manifestations of congenital toxoplasmosis in infancy: a cohort study in 13 European centres. Acta Paediatr 2005; 94: 1721-1731
- 53 Schuster S, Janatzek S, Chittka L. IGeLMonitor- Evidenz ausführlich – Toxoplasmose-Test in der Schwangerschaft. Accessed September 10, 2022 at: https://www.igel-monitor.de/fileadmin/user_upload/Toxoplasmosetest_Schwangerschaft_Evidenz_ausfuehrlich.pdf
- 54 Katlama C, De Wit S, OʼDoherty E. et al. Pyrimethamine-clindamycin vs. pyrimethamine-sulfadiazine as acute and long-term therapy for toxoplasmic encephalitis in patients with AIDS. Clin Infect Dis 1996; 22: 268-275
- 55 Araujo FG, Remington JS. Effect of Clindamycin on Acute and Chronic Toxoplasmosis in Mice. Antimicrob Agents Chemother 1974; 5: 647-651
- 56 Buonsenso D, Pata D, Turriziani Colonna A. et al. Spyramicine and Trimethoprim-Sulfamethoxazole Combination to Prevent Mother-To-Fetus Transmission of Toxoplasma gondii Infection in Pregnant Women: A 28-Years Single-center Experience. Pediatr Infect Dis J 2022; 41: e223-e227
- 57 EACSociety. EACS Guidelines. Accessed September 17, 2022 at: https://www.eacsociety.org/guidelines/eacs-guidelines/
- 58 Reiter-Owona I, Hlobil H, Enders M. et al. Sulfadiazine plasma concentrations in women with pregnancy-acquired compared to ocular toxoplasmosis under pyrimethamine and sulfadiazine therapy: a case-control study. Eur J Med Res 2020; 25: 59
- 59 Peytavin G, Leng JJ, Forestier F. et al. Placental transfer of pyrimethamine studied in an ex vivo placental perfusion model. Biol Neonate 2000; 78: 83-85
- 60 Wehbe K, Pencole L, Lhuaire M. et al. Hygiene measures as primary prevention of toxoplasmosis during pregnancy: A systematic review. J Gynecol Obstet Hum Reprod 2022; 51: 102300
- 61 Gemeinsamer Bundesausschuss. Mutterschafts-Richtlinien. 2021. Accessed April 18, 2023 at: https://www.g-ba.de/downloads/62-492-2676/Mu-RL_2021-09-16_iK-2022-01-01.pdf
- 62 Prusa A-R, Kasper DC, Sawers L. et al. Congenital toxoplasmosis in Austria: Prenatal screening for prevention is cost-saving. PLoS Negl Trop Dis 2017; 11: e0005648
- 63 SGGG. Expertenbrief 31 – Verzicht auf das Toxoplasmose-Screening in der Schwangerschaft – kurze zusammenfassende Begründung. 2010. Accessed September 17, 2022 at: https://www.sggg.ch/fileadmin/user_upload/PDF/31_Toxoplasmose-Screening_2010.pdf
- 64 Wallon M, Kieffer F, Huissoud C. et al. Cesarean delivery or induction of labor does not prevent vertical transmission of toxoplasmosis in late pregnancy. Int J Gynaecol Obstet 2015; 129: 176-177
- 65 Arbeitsgruppe Infektiologie der Österreichischen Gesellschaft für Kinderheilkunde. Österreichische Richtlinie für das Toxoplasmose-Screening in der Schwangerschaft und frühen Kindheit. 2013. Accessed January 21, 2021 at: https://www.oeghmp.at/media/richtlinie_toxoplasmose-screening.pdf
- 66 Wichtige humane Parasitosen: Toxoplasmose. Z Gastroenterol 2020; 58: 742-746































